 研发追踪
研发追踪
 药明康德
药明康德
 2021.10.15
2021.10.15
 1846
1846
2021年10月13日,默沙东(MSD)公司宣布,美国FDA批准PD-1抑制剂帕博利珠单抗(pembrolizumab,英文商品名为Keytruda)与含铂化疗联用,加或不加贝伐珠单抗(bevacizumab),一线治疗肿瘤表达PD-L1(CPS分数≥1)的持续性、复发性或转移性宫颈癌患者。新闻稿指出,这是获批一线治疗这些患者的首个抗PD-1抗体组合疗法。

该批准基于一项多中心、随机双盲、含安慰剂对照的关键性3期临床试验的积极结果。该试验共入组617名持续性、复发性或转移性宫颈癌成人患者(无论PD-L1状态如何),这些患者没有接受过全身化疗。试验结果显示,对于表达PD-L1的肿瘤患者(CPS≥1.n=548):
与化疗相比,帕博利珠单抗+化疗将患者死亡风险降低36%(HR=0.64;95% CI:0.50.0.81;p=0.0001)。
帕博利珠单抗+化疗组的中位PFS为10.4个月,化疗组为8.2个月(HR=0.62;95% CI:0.50.0.77;p<0.0001)。
帕博利珠单抗+化疗组和化疗组的客观缓解率分别为68%和50%。
帕博利珠单抗+化疗和化疗组的中位缓解持续时间分别为18.0个月和10.4个月。
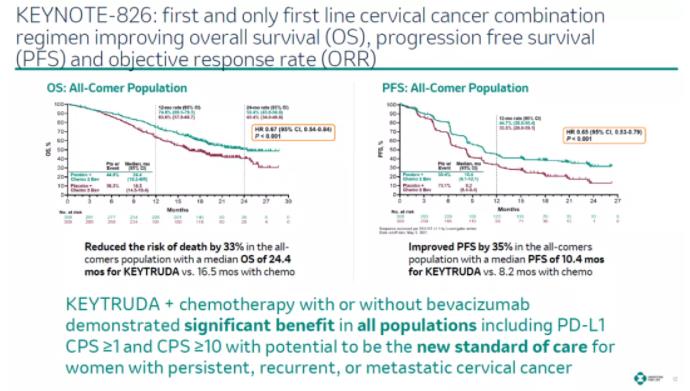
▲帕博利珠单抗/化疗组合显著提高患者总生存期和无进展生存期(图片来源:默沙东官网)
“宫颈癌通常影响更年轻的女性,不幸的是,确诊患有持续性、复发性或转移性宫颈癌的女性通常生存率较低。”亚利桑那大学医学院的肿瘤学家Bradley Monk博士说,“这一疾病过去7年没有新的一线获批疗法。我很高兴今天Keytruda组合疗法获得批准,给合适的患者带来了一个新治疗选择。”
参考资料:
[1] FDA approves pembrolizumab combination for the first-line treatment of cervical cancer. Retrieved October 13. 2021. from https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-combination-first-line-treatment-cervical-cancer
[2] FDA Approves Merck’s KEYTRUDA® (pembrolizumab) Plus Chemotherapy, With or Without Bevacizumab, as Treatment for Patients With Persistent, Recurrent or Metastatic Cervical Cancer Whose Tumors Express PD-L1 (CPS ≥1). Retrieved October 13. 2021. from https://www.businesswire.com/news/home/20211013006053/en

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34299
34299

 医药地理
医药地理
 2018.10.22
2018.10.22
 18804
18804

 医谷
医谷
 2019.03.18
2019.03.18
 18727
18727