 研发追踪
研发追踪
 医麦客
医麦客
 2023.11.06
2023.11.06
 1924
1924
2023年11月2日/医麦客新闻 eMedClub News/--2023年10月31日,Chimeric Therapeutics宣布,美国FDA已经批准其CDH17靶向CAR-T细胞疗法的研究新药(IND)申请,未来将计划在2024年开展一项针对晚期结肠直肠癌、胃癌和神经内分泌肿瘤患者的多中心、开放标签1A/B期临床试验中研究CHM 2101。
CHM 2101的临床项目建立可以追溯到去年。2022年3月21日,宾夕法尼亚大学医学院的Dr Xianxin Hua团队在《Nature Cancer》上发表重磅论文,研究者们开发了一款针对CDH17的VHH1-CAR T细胞,在肿瘤异种移植或原发小鼠模型中,该疗法完全消除了表达CDH17的神经内分泌肿瘤(NET)和胃肠道癌细胞(GIC),且对不表达CDH17的正常细胞无损伤。

▲ 图片来源:《Nature Cancer》
CDH17是一种与最常见胃肠道肿瘤(包括结肠直肠癌、胃癌和神经内分泌肿瘤)的不良预后和转移相关的癌症靶点。值得注意的是,CDH17 CAR-T相比其他靶向的同类疗法表现出优越的安全性,对同样表达CDH17的正常肠上皮细胞无毒性,仅仅杀伤癌细胞,不会伤害正常组织。接受治疗的小鼠的小肠和结肠完好无损,其胃、胰腺、心脏、肝脏和肾脏中也未观察到明显的结构损伤。这可能是因为CDH17被隔离并隐藏于肠上皮细胞之间的紧密连接处的健康组织间,而CAR-T细胞不能到达或结合到该位置,表明CDH17是一个潜在的较为安全的实体瘤靶点。

▲胃肠道癌细胞上的CDH17模式图 图片来源:Chimeric 官网
随后,Chimeric Therapeutics与宾夕法尼亚大学加深合作关系。Chimeric从宾大获得非独家授权的第三代慢病毒载体系统使用,以开发和商业化公司靶向CDH17的CAR-T细胞疗法CHM 2101。

▲CHM 2101作用 图片来源:Chimeric 官网
胃肠道肿瘤(GIC,包括胃癌、胰腺癌、结直肠癌)和神经内分泌肿瘤(NET)在转移后通常是致命的。全世界每年约有500万例GIC新病例,GIC相关死亡占所有癌症相关死亡的35%。GIC的传统治疗方法包括手术、化疗和分子靶向疗法,但转移性胃肠道癌患者的总体生存率仍然很低。
从2022年初在临床前研究中发现CDH17靶点并开发该靶点CAR-T疗法,再到如今将其用于胃肠道癌症和神经内分泌肿瘤患者,启动临床试验,这是开发全新CAR-T疗法的关键一步,为现有疗法难以治愈的癌症患者带来了新的希望。基于此特点,Chimeric Therapeutics还开发了该靶点的CAR-NK细胞疗法CHM2301。
两款双抗,开启CDH17研发路
目前针对CDH17靶点的药物并不多,且均处于早临床或临床前研发阶段,其中进展最快的是ARB202和BI-905711两款双抗药物。
今年8月2日,Arbele公司在ASCO突破性会议上公布了其首款CDH17xCD3双特异性T细胞参与抗体ARB 202的早期安全性数据,该药品曾在2022年8月在澳大利亚完成I期首次临床试验首例患者给药。

▲ARB 202结构 图片来源:Arbele官网
ARB 202是一种针对晚期胃肠道癌症的新型免疫疗法,既能靶向胃肠道肿瘤的CD17,也能靶向T细胞上的CD3。ARB 202对CDH17和CD3独特的差异结合亲和力使其具有高特异性和细胞毒性,同时避免了T细胞的“脱靶”过激活。来自1a期研究的初步数据表明——ARB 202在血液循环中的耐受性Cmax高达150ng/ml,这表示在这些浓度下没有临床显著的脱靶T细胞活化。
Boehringer Ingelheim的BI-905711,是靶向TRAILR2和CDH17的四价双抗,TRAILR2与CDH17交联诱导CDH17依赖性TRAILR2聚集,在共表达TRAILR2和CDH17的肿瘤细胞中诱导选择性凋亡。已于2020年9月开展I期临床试验。在ESMO大会上 Boehringer Ingelheim公布了BI 905711在临床I期治疗胃肠道肿瘤的结果,入组45例患者,观察到12例患者达SD,安全性良好。
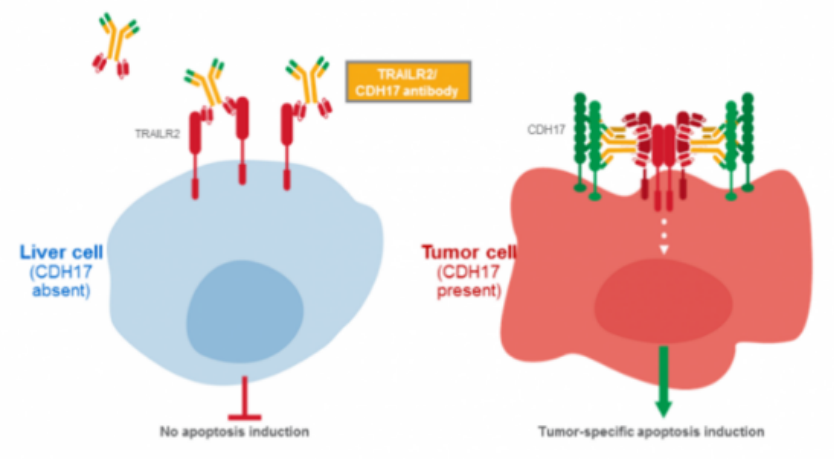
▲肿瘤细胞中TRAILR2/CDH17作用机制 图片来源:Boehringer官网
Chimeric主打实体瘤靶点上的突破创新
值得一提的是,2021年1月,Chimeric Therapeutics登陆澳交所,上市首日股价暴涨近50%,资本市场非常看好Chimeric在实体瘤靶点上的创新,将开创CAR-T研发的新格局。
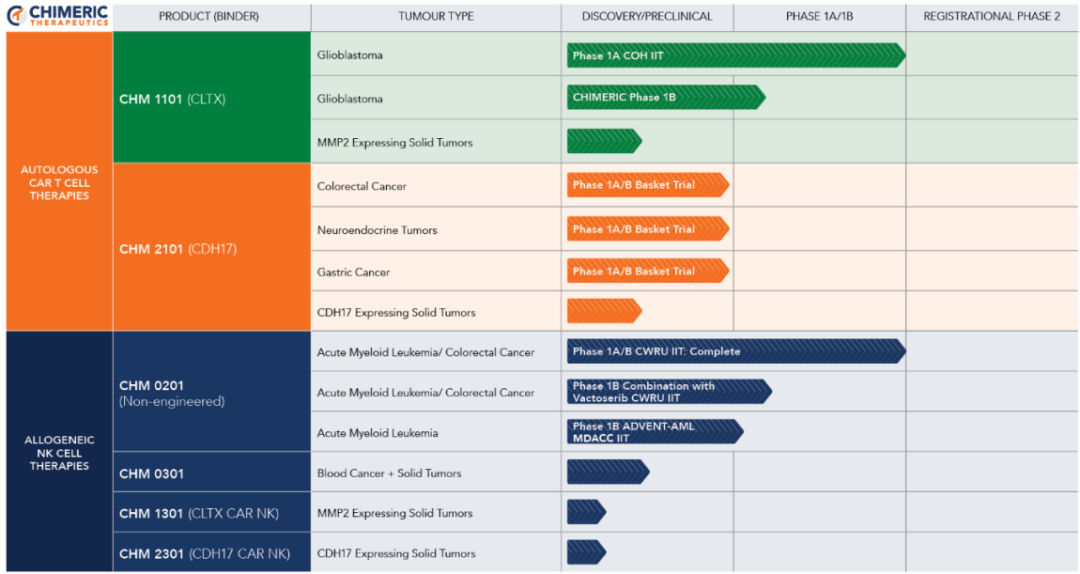
▲ Chimeric在研管线 图片来源:Chimeric官网
Chimeric 除了靶向CDH17的CAR-T CHM 2101外,还有另外一款独创的新型CAR-T细胞疗法,即基于氯毒素(CLTX)的CAR-T,CHM 1101。Chimeric利用蝎毒的肽成分氯毒素(CLTX)作为嵌合抗原受体(CAR)的肿瘤靶向成分,来引导T细胞靶向脑肿瘤细胞,有可能解决复发性或进行性胶质母细胞瘤患者的高度未满足的医疗需求。
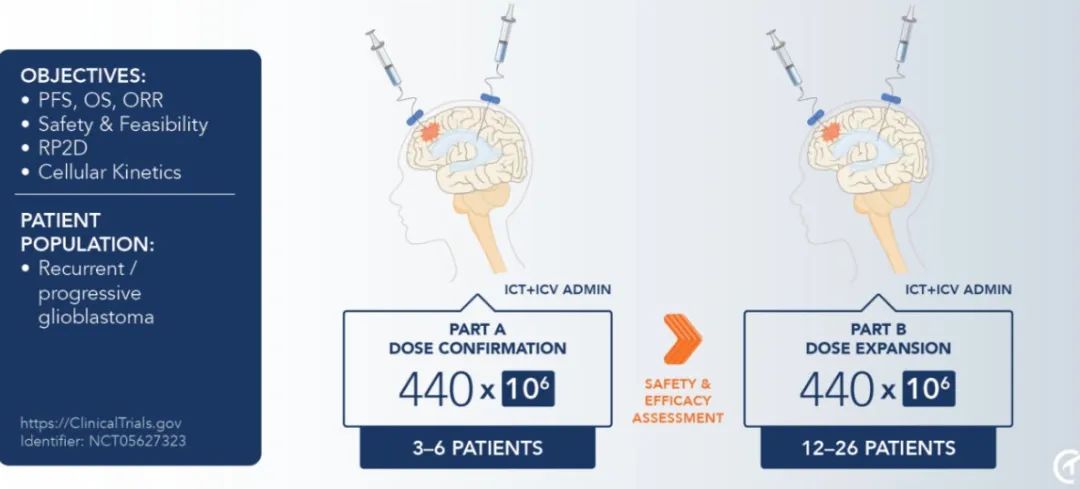
▲ 图片来源:Chimeric官网
2023年6月4日,Chimeric 宣布启动一项针对复发性和/或进行性多型胶质母细胞瘤(GBM)患者的1B期临床试验,以评估该公司首个CLTX CAR-T细胞疗法CHM 1101的安全性和有效性。这项多中心试验将使Chimeric公司能够更快地推进CHM 1101的开发,并在临床结果的支持下为下一阶段的开发做好准备。CHM 1101来源于蝎子毒液的氯毒素(CLTX)先前曾被证明能与胶质母细胞瘤细胞结合,已被用作显像剂指导胶质母细胞瘤切除手术,有望克服传统CAR-T靶向实体瘤时,无法解决肿瘤异质性和抗原逃逸的局限。
结语
虽然在研的临床阶段管线并不算多,但已有两款同类首款靶点CAR-T获得了积极的临床前数据,并逐步向CAR-NK扩展。Chimeric的创新研发能力将在CAR-T的CD19、BCMA靶点内卷中开辟新的道路,并将适应症专注于占90%癌症的实体瘤,未来的市场潜力不可限量。相信在未来攻克实体瘤的创新生物药大军中,Chimeric或将是不可避免被提及的名字。

 新浪医药
新浪医药
 2018.07.12
2018.07.12
 34594
34594

 医谷
医谷
 2019.03.18
2019.03.18
 18925
18925

 医药地理
医药地理
 2018.10.22
2018.10.22
 18910
18910