 产业资讯
产业资讯
 医麦客
医麦客
 2024.04.24
2024.04.24
 145
145
近年来,生物创新药蓬勃发展,在多个领域中取得了突破。其中,细胞治疗领域已上市的CAR-T疗法已经达到11款,海外的6款在2023年全年销售额达到了37.13亿美元,销售额稳步增长。并且,今年首个TIL疗法的获批上市,且TCR-T疗法上市在即,γδ-T、双阴性T细胞(DNT)等不同类型的T细胞疗法也已经在临床研究阶段中显示出初步的疗效和良好的安全性。据Pharma projects数据库显示,截至2023年6月,全球生物制药行业管线中有3771种细胞和基因疗法正在积极开发,细胞疗法有1989种,占比过半,未来发展潜力巨大[1]。
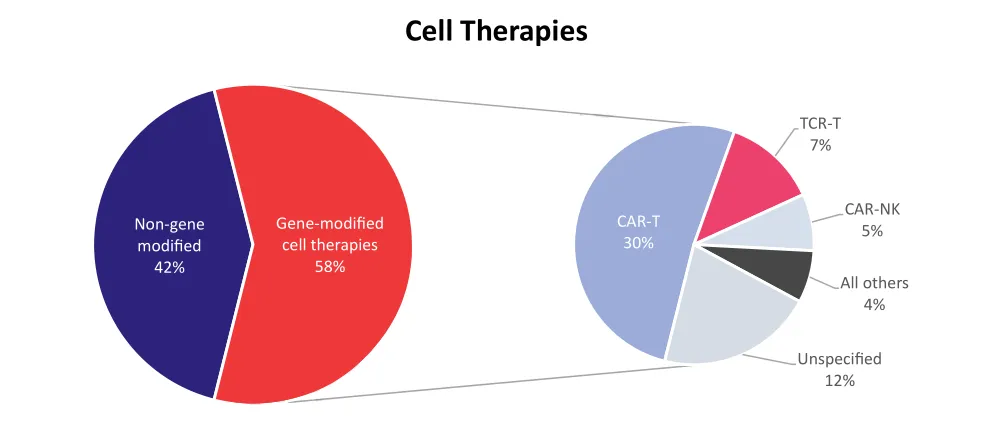
(细胞疗法在研管线及类型,来源:参考资料1)
今年初起,生物创新药迎来了明显的复苏迹象,1月以来已经发生了多起融资和BD事件,仅细胞治疗领域在开年后两个月的潜在总金额就超过了30亿美元,为全年发展奠定下了基调
在全球生物创新药快速放量和持续发展的背景下,作为上游原材料的关键组成部分、生物医药行业发展的基石——培养基,也有望迎来快速增长阶段。据沙利文数据显示,2021年全球培养基规模达到21亿美元,并预计将以10.7%的年均复合增速增长至2026年的35亿美元[2]。而国内创新药具有起步晚发展快的特点,对培养基需求的增长高于全球平均增速,具有更加广阔的市场空间。
推陈出新,无血清培养基渐成行业主流
细胞培养基的分类方式众多,根据组成成分不同可以分为含血清培养基、低血清培养基、无血清培养基、无蛋白培养基等。这一行业从二十世纪50年代发展至今,共经历了四大时期,由血清培养基逐渐转向无血清培养基,并进一步开发出了化学成分限定培养基,在21世纪以后,无动物源的化学成分限定的培养基持续优化,品牌效应出现,同时,更大规模的生产需求也对培养基提出了更高的要求。
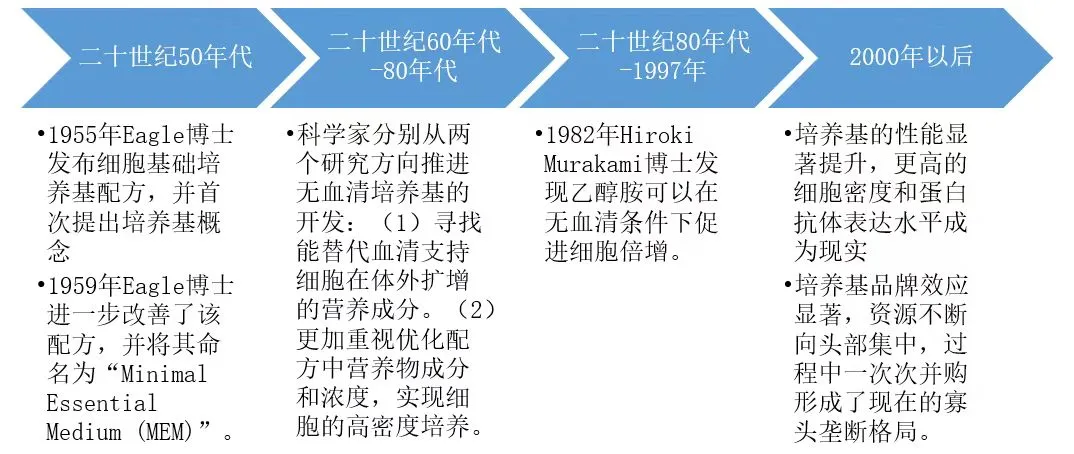
(培养基发展阶段,来源:据公开资料整理)
其中,血清培养基开发时间较早,血清中包含了多种生长因子和激素,能够提供丰富的营养物质,刺激细胞生长和发挥功能,不过也存在着较多局限性。血清成分复杂,包含了几百种物质,但目前对血清的准确成分、含量以及作用机制尚不清楚,而这种未知对研究所带来的影响难以评估。
而无血清培养基不含动物成分、无外源污染、组分稳定,支持大规模生产,批次间稳定性高,能够提升细胞培养和研究结果的重复性;同时,无血清培养基可提高产品的表达水平,一方面提高了研发和生产的效率,另一方面方便下游产物分离和纯化,在科研及商业领域的应用愈加广泛。无血清、化学成分确定的培养基逐渐成为当下以及未来长时间内的主流培养基,也是目前公认的安全且理想的培养基。
基于无血清培养基的这些特性,其也被广泛用于多种领域。在T细胞免疫治疗领域中,培养基的择优选择能够有效提升各类细胞的扩增效率,能够调节细胞的表型和转导率。在研发端,培养基会直接影响研发进度和成功率;在生产端,培养基则会影响生产效率和终产品质量,进而可能影响产品审批时间。因此,选择合适可靠的培养基至关重要。
高壁垒之下术业有专攻,
培养基选择助力事半功倍
当下,无血清培养基已然在配方开发、生产等方面形成了高度的行业壁垒,且品牌效应显著增强。在配方方面,无血清培养基的研发不仅要求企业深入了解细胞生长和代谢的复杂机制,还需精确掌握各种营养成分之间的相互作用及其对细胞生长的影响,配方上细微的差距会影响细胞的状态。这也使得无血清培养基的配方设计具有高度专业化的特点,属于企业的技术秘密,也是企业的核心竞争力之一。
龙沙(Lonza)推出的TheraPEAK™ T-VIVO™细胞培养基就是采用化学成分明确的新型配方,消除了动物成分,仅使用重组蛋白,能够提高性能、提供更好的一致性和过程控制,可以加速临床前开发、监管审批和疗法生产。值得一提的是,这一培养基不同于其他无血清培养基,其无需添加人血清或血清组分即可实现高性能。
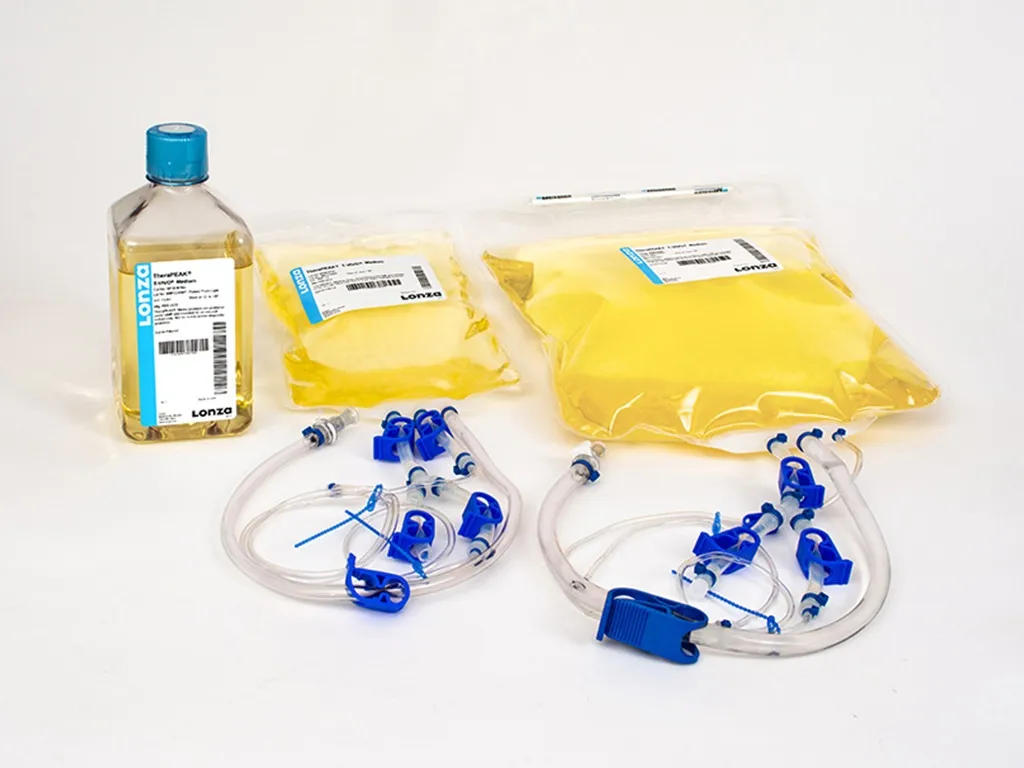
Scientific Reports研究结果表明,使用TheraPEAK™ T-VIVO™细胞培养基在生成高质量、高功能性CAR-T细胞方面显示出优越性,满足了包括T细胞生产过程中,高扩增倍数、高活性、适宜的激活状态以及有效的靶细胞杀伤等关键要求[3]。并且,TheraPEAK™ T-VIVO™培养基支持多种T细胞类型的培养和扩增,包括T细胞、CAR-T细胞、TCR-T细胞、γδ-T细胞、外周血淋巴细胞(PBL)、肿瘤浸润淋巴细胞(TIL);也适配多种细胞培养平台,包括方瓶、转瓶、透气型细胞培养瓶、波浪式反应器、搅拌罐式反应器和Cocoon®平台等。
在生产方面,生产工艺的精细化、标准化和规范化不仅能够确保培养基质量的稳定性和一致性,还能够提高生产效率,降低成本。因此,先进的生产工艺也是无血清培养基行业的壁垒之一,并非是每个企业都能掌握。同时,培养基的生产也考验着企业对供应链的把握和质量管理体系的建设,不同供应商或者同一供应商的不同批次原料均可能会对最终生产出来的培养基产生影响,进而影响到细胞生长结果。
高行业壁垒也促使品牌黏性增强,客户往往倾向于选择经过验证的,具有可靠配方和大规模生产工艺的企业。在去年发布的《自体CAR-T细胞治疗产品药学变更研究的问题与解答》提到原则上应在确证性临床试验阶段开始前完成重大药学变更,锁定生产工艺,使确证性临床试验阶段的场地、产能、工艺、物料、检测、质量等方面与商业化生产密切衔接。而培养基就属于关键生产用料,培养基的变更如经评估可能影响CAR-T细胞的质量,则需要开展可比性研究。
这也意味着,细胞疗法研发企业与机构要谨慎选择培养基,且在选定后一般不会轻易发生更换。而知名培养基厂商凭借着优秀的配方、先进的生产工艺和完善的质量管理体系,既能够符合企业的筛选标准,也满足日益严格的生物安全和法规要求,能够协同推动行业发展。

龙沙作为世界知名细胞培养基制造商,其培养基TheraPEAK™ T-VIVO™由具有ISO 13485认证、符合GMP指南生产规范的工厂生产,污染风险极小,且该培养基具有可追溯性文件(包括《检验报告》和《药物主文件》等),减少了可追溯性和文档负担,简化了流程并支持合规性,促进了从临床前开发到生产的规模放大。另外,龙沙具有稳定的大规模供应能力,也满足了未来企业在商业化阶段的需求。
注入新活力,续写新篇章
在细胞治疗乃至整个生物创新药发展越来越快的时代,培养基的推陈出新有助于为行业发展注入了新的活力,也满足了日益增长的复杂且精细的细胞培养需求,同时在一定程度上能够促进企业达到降本增效的目的。未来,培养基的革新将继续为行业的进步续写新篇章。
参考资料:
1、Chancellor D, Barrett D, Nguyen-Jatkoe L, Millington S, Eckhardt F. The state of cell and gene therapy in 2023. Mol Ther. 2023;31(12):3376-3388. doi:10.1016/j.ymthe.2023.11.001
2、《【医药】生命科学上游系列报告之一,细胞培养基:小赛道,大未来_20220807》
3、von Auw, N., Serfling, R., Kitte, R. et al. Comparison of two lab-scale protocols for enhanced mRNA-based CAR-T cell generation and functionality. Sci Rep 13, 18160 (2023). https://doi.org/10.1038/s41598-023-45197-x

 CPhI制药在线
CPhI制药在线
 2018.07.24
2018.07.24
 49776
49776

 艾美仕
艾美仕
 2018.07.09
2018.07.09
 34772
34772


 2014.03.11
2014.03.11
 31159
31159