 产业资讯
产业资讯
 摩熵医药
摩熵医药  2026-04-11
2026-04-11
 1601
1601
短短九个月内,一款新药在中国市场完成了从首次申报到冲击一线治疗的关键跃进。
2026年4月9日,CDE官网公示,拜耳的肺癌新药塞伐艾替尼片(sevabertinib)拟纳入优先审评程序,用于一线治疗携带HER2激活突变的晚期非小细胞肺癌(NSCLC)成人患者。这是继2025年7月其首次提交上市申请后,该药在中国递交的第二个新适应症申请,标志着其临床应用阵线正加速向前推移。

截图来源:CDE官网
01
从二线到一线,9个月内加速推进上市
塞伐艾替尼片(sevabertinib)是拜耳研发的一款口服、非共价、可逆选择性酪氨酸激酶抑制剂,可抑制携带EGFR及HER2突变(包括HER2 exon 20插入突变)的肿瘤生长。2025年7月,该药首次在中国申报上市,用于既往接受过一种系统治疗的HER2突变晚期NSCLC患者。此次将适应症前移至一线治疗,显示拜耳正加速推进该药在更早治疗阶段的应用布局。
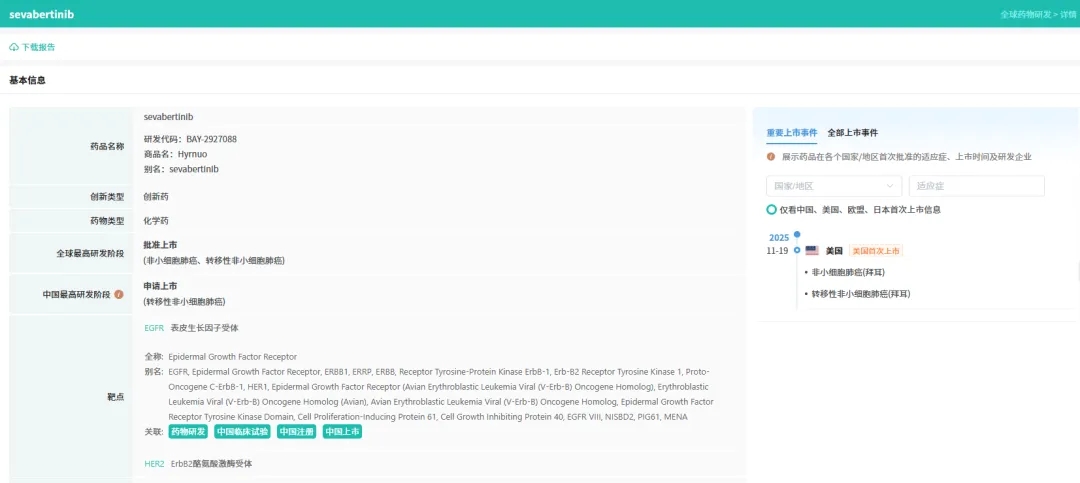
截图来源:全球药物研发数据库(查数据.找摩熵)
2025年11月19日,塞伐艾替尼已在美国获批上市,用于治疗经FDA批准的伴随诊断证实携带HER2酪氨酸激酶结构域激活突变、且接受过系统治疗的局部晚期或转移性非鳞状NSCLC成人患者。
从首次在华申报到此次一线适应症纳入优先审评,仅间隔不到9个月,体现了监管部门对填补临床空白品种的加速支持,也反映了企业在关键适应症上快速推进的注册策略。
02
约8.4万全球年新发患者,一线仍缺靶向药
在非小细胞肺癌(NSCLC)患者中,HER2基因突变的发生率约为2%-4%,该突变更常见于女性、年轻及不吸烟人群。据统计,全球每年新增的HER2突变NSCLC病例约为8.4万例,但目前尚无针对该突变的靶向药物获批。
一线治疗,是一片价值巨大且完全空白的靶向药市场。若塞伐艾替尼一线适应症成功获批,将填补该领域靶向治疗空白,为患者提供新的治疗选择。
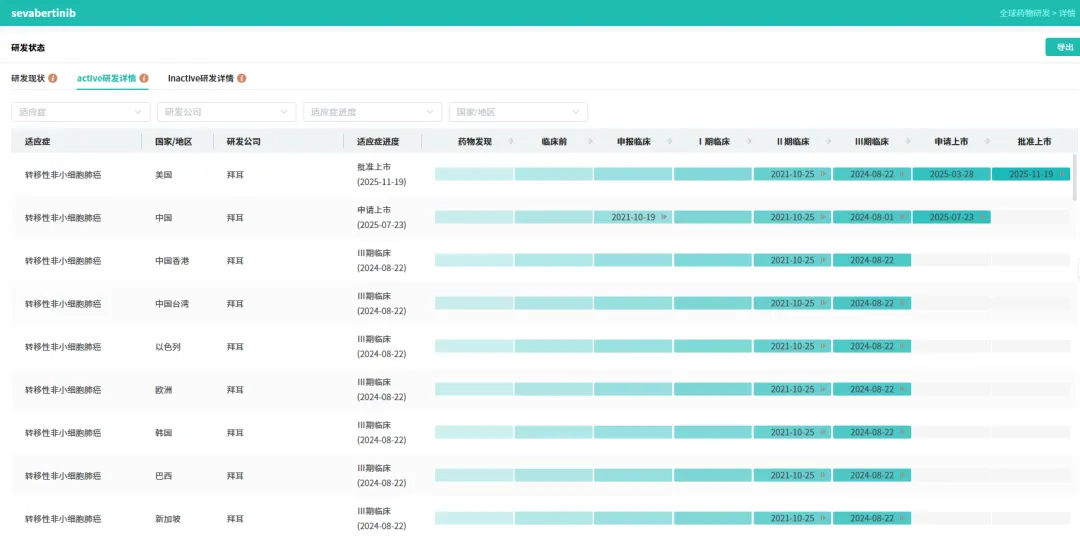
截图来源:全球药物研发数据库(查数据.找摩熵)
在HER2突变NSCLC的二线治疗中,阿斯利康/第一三共的抗体偶联药物(ADC)德曲妥珠单抗是目前的标准方案之一,客观缓解率(ORR)约50%-60%。但ADC类药物需静脉输注,且存在间质性肺炎等风险。相比之下,口服TKI在用药便利性上具有明显优势。
目前全球仅有两款口服HER2 TKI获批,分别为拜耳的塞伐艾替尼和勃林格殷格翰的宗格替尼。两者疗效数据相近,拜耳正积极推进一线治疗注册,有望在治疗阶段上取得领先。
03
国内已有3款疗法获批,口服TKI赛道竞争升温
目前国内已有3款针对HER2突变NSCLC的靶向疗法获批上市,包括:恒瑞医药的瑞康曲妥珠单抗注射剂;第一三共/阿斯利康的德曲妥珠单抗注射剂;勃林格殷格翰/中国生物制药的宗艾替尼口服片剂。

截图来源:全球药物研发数据库(查数据.找摩熵)
若塞伐艾替尼顺利获批,将成为国内第4款针对HER2突变NSCLC的靶向疗法,也是第2款口服HER2靶向药物,进一步丰富患者的治疗选择。
结语
从二线到一线,塞伐艾替尼在不到9个月内完成适应症拓展申报并获优先审评资格,凸显了临床需求与审评审批的双向加速。
随着塞伐艾替尼等新一代口服TKI的推进,HER2突变NSCLC靶向治疗前线化、口服化趋势日益明显。未来2-3年,该领域有望从“缺药”走向“多药可选”,为患者带来更具便利性与精准性的治疗新方案。

 产业资讯
产业资讯
 医曜
医曜  2026-06-11
2026-06-11
 396
396

 产业资讯
产业资讯
 药智网
药智网  2026-06-11
2026-06-11
 430
430

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-06-11
2026-06-11
 404
404
 热门资讯
热门资讯