 产业资讯
产业资讯
 药智数据
药智数据  2026-04-14
2026-04-14
 1513
1513
01
临床试验类型分布情况
2026年3月,据药智数据企业版【中国临床试验】数据库显示CDE公示登记的药物临床试验共计498个临床试验登记。其中,化药临床试验以345项占据主要,生物制品和中药则分别为142项和11项。
在试验分期方面,占比最大的是“其他”临床试验,达到了36.3%,总计181项试验,且这些试验中化学药物的生物等效性试验占绝大多数。其次是“1期”试验,合计171项研究,另外2期和3期试验数量分别为96、69项,4期临床试验仅有8项。
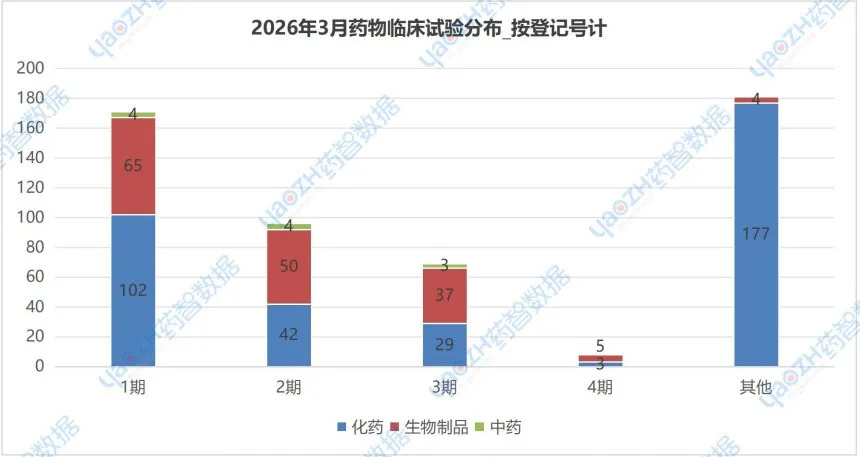
注:由于存在同一临床试验属于多个临床分期的情况,所以上述统计数量会多于临床试验总数
02
药物临床试验品种分析
在2026年3月CDE登记的药物临床试验品种top10榜单中,“非奈利酮片”以12个登记试验位列榜首,且都为生物等效性临床试验。“非奈利酮片”的12个临床试验分别由浙江兄弟药业有限公司、江苏吴中医药集团有限公司苏州制药厂、齐鲁制药有限公司等公司申办,针对的临床试验适应症都为“与2型糖尿病相关的慢性肾脏病成人患者(伴白蛋白尿),以降低肾小球滤过率估计值(eGFR)持续下降、终末期肾病、心血管死亡和因心力衰竭住院的风险”。“多替诺雷片”以8个临床试验位列第二,均为生物等效性临床试验。
更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
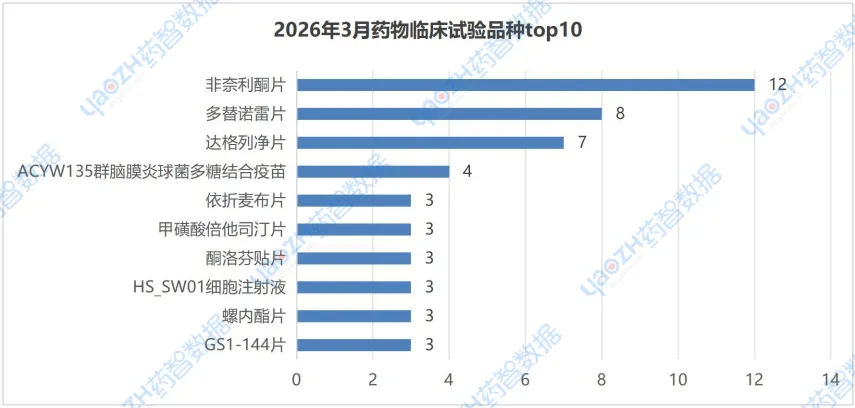
注:由于存在并列情况,所以上述排行可能不止10个
03
药物临床试验申报单位分析
在2026年3月的CDE药物临床试验申办单位排行榜中,“齐鲁制药有限公司”以12个临床登记试验位列榜首,“齐鲁制药有限公司”的12项试验涵盖了10个不同品种的临床试验,既有新药临床试验,也有生物等效性试验,具体为“非奈利酮片、多替诺雷片、艾地苯醌片、QL2109 注射液”等;“北京科兴中维生物技术有限公司”以5个临床登记试验位列第二,且5个临床登记试验全部为新药临床试验。
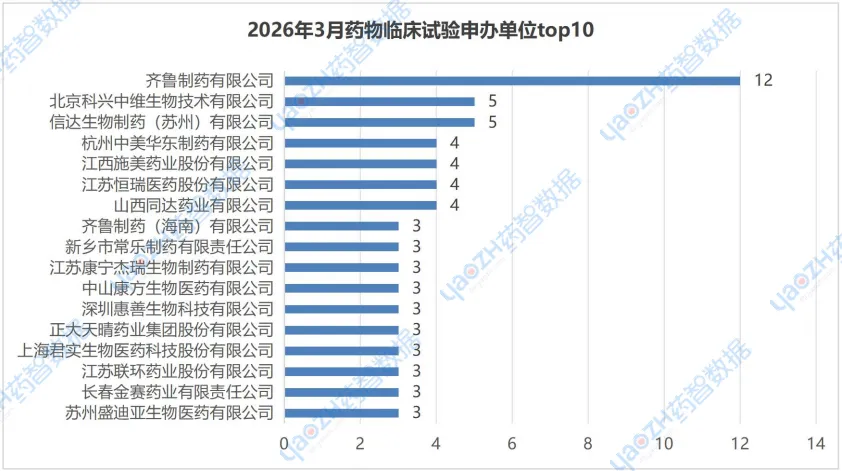
注:由于存在并列情况,所以上述排行可能不止10个
04
药物临床试验机构分析
在2026年3月的CDE药物临床试验登记公示中,“北京大学第一医院”以牵头13个临床试验位列榜首,且这13个临床试验绝大多数为新药临床试验。
“北京大学肿瘤医院”则以牵头11个临床试验位列第二,且均为新药临床试验。更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
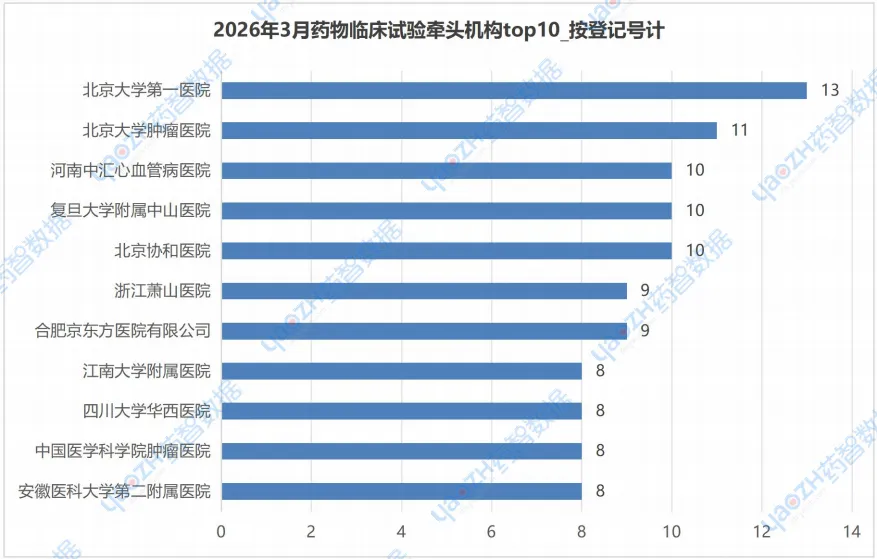
注:由于存在并列情况,所以上述排行可能不止10个
05
临床试验省份分布情况
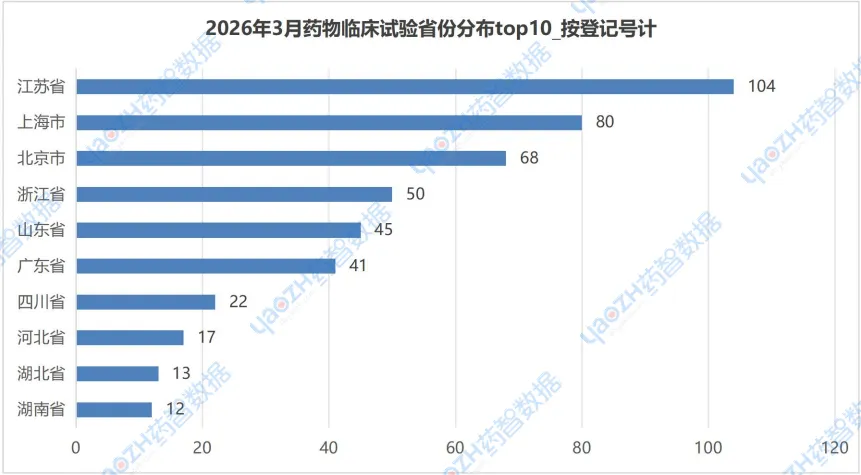
在2026年3月的CDE药物临床试验登记公示中,按申办单位所在地区统计,临床试验省份分布见下图,江苏以104个临床试验登记位居首位,上海和北京位列第二和第三。更多详细信息,请详见下图或访问药智数据企业版【中国临床试验】数据库进行查询。
06
临床试验关键事件
1、TVAX-008(治疗性乙肝疫苗)III期临床完成首例入组
TVAX-008是一款旨在实现慢性乙肝(CHB)“功能性治愈”的创新治疗性疫苗。与传统核苷(酸)类似物(抑制病毒复制)不同,该疫苗的设计逻辑是通过特异性抗原表位刺激,重建宿主针对乙肝病毒的特异性T细胞和B细胞免疫应答,从而打破患者的免疫耐受状态。该项目III期临床试验在全国组长单位北京大学第一医院(其在肝病及乙肝临床研究领域具有顶尖权威性)顺利完成首例受试者入组,标志着这一重磅品种正式进入大规模确证性临床阶段。基于早期临床中展现出的优异免疫激活效果和安全性,TVAX-008此前已被CDE正式纳入“突破性治疗药物”品种。此次III期试验预计将入组更大规模的慢乙肝患者群体,其核心终点大概率聚焦于临床业界公认的“功能性治愈”金标准——治疗结束时或停药后的HBsAg(乙肝表面抗原)清除率。该入组的推进意味着国产乙肝功能性治愈管线迈出了关键一步。
2、εPA-44被NMPA纳入1类治疗用生物制品,属于另一技术路径的治疗性乙肝疫苗
该药物在结构设计上侧重于优化抗原递呈效率,以期在体内诱导更强效、更持久的特异性免疫反应。3月24日,其新增适应症的临床试验申请(IND)正式获得NMPA受理。
临床数据支撑与后续展望:在前期已完成的II期临床试验中,εPA-44在特定慢乙肝队列中展现出了令人鼓舞的有效性信号,尤其是在促使部分患者HBsAg滴度显著下降乃至清除方面表现出潜力。此次申请新增适应症,通常意味着企业将基于前期数据,进一步探索该药物在不同乙肝患者亚群(如HBeAg阴性/阳性患者、低病毒血症患者等)中的疗效边界,或是探索与现有直接抗病毒药物(DAA)的联合用药方案,以扩大临床受益人群。
3、和铂医药/科伦博泰:长效双抗HBM7575/SKB575(特应性皮炎)IND获批,即将启动针对中重度特应性皮炎(AD)的中国临床试验
差异化优势与临床意义:当前AD生物制剂赛道竞争激烈(如IL-4Rα、IL-13靶点已有多款重磅药物上市)。该双抗的临床优势在于:一方面,通过双管齐下阻断TSLP等多条炎症级联反应的上游信号,有望覆盖更广泛的炎症表型,解决部分患者对现有单抗响应不足的问题;另一方面,“长效”设计有望将给药频率从常规的每两周一次延长至每月甚至每季度一次,大幅提升患者的依从性。此次IND获批,标志着该极具商业潜力的自免双抗正式迈入人体概念验证阶段。

 产业资讯
产业资讯
 医曜
医曜  2026-06-11
2026-06-11
 394
394

 产业资讯
产业资讯
 药智网
药智网  2026-06-11
2026-06-11
 428
428

 产业资讯
产业资讯
 生物药大时代
生物药大时代  2026-06-11
2026-06-11
 402
402
 热门资讯
热门资讯