 研发追踪
研发追踪
 瞪羚社
瞪羚社  2026-04-18
2026-04-18
 110
110
大家可能都没注意到,异体CAR-T迎来一个具备强意义的历史性突破。
Allogene Therapeutics宣布了Cema-cel用于一线巩固治疗大B细胞淋巴瘤(LBCL)ALPHA3研究的中期无效性分析数据,数据显示:Cema-cel治疗组的微小残留病(MRD)清除率达到58%,远远超出安慰剂组17%的清除率,且超过了当初管理层设定的25-30%的目标值,同时安全性也是非常之好。
值得注意的是,Cema-cel是一种全球临床进度领先的抗同种异体(通用型)CD19 CAR-T细胞疗法,并且ALPHA3研究是一项注册性二期(成功有望直接递交BLA),同时也是全球首个针对作为LBCL一线巩固治疗的同种异体CAR-T研究(差异化于大量复发/难治性末线治疗研究)。
尽管从Allogene市场表现在数据公布后大涨随后回落,但公司近6个月的股价涨幅已经超过70%。
这份ALPHA3研究的中期无效性分析数据意义非凡,不仅代表通用型CAR-T迈向早线治疗更进一步,同时也代表这个领域离成药越来越近。
01
全球首创的历史意义
Allogene的Cema-cel开辟了一个全新的治疗窗口。
目前获批的自体CAR-T(Yescarta、Breyanzi、Kymriah)全部用于2L+复发/难治LBCL,基本上治疗决策主要依据影像学评估(PET-CT)确认疾病复发/进展后才会启动CAR-T治疗(一线治疗→影像学CR→观察→等复发→再用CAR-T)。
大家可以注意到ALPHA3研究中期分析是以MRD为指导的数据分析,一般在CAR-T用于事后监测/研究分析(用于评估CAR-T治疗反应深度),而MRD在ALPHA3研究创新性的用于患者筛选,这意味着他不再是在LBCL患者治疗复发后和自体CAR-T竞争,开辟了一个全新的治疗窗口(一线治疗→MRD检测→MRD阳性患者直接用cema-cel巩固→预防复发)。
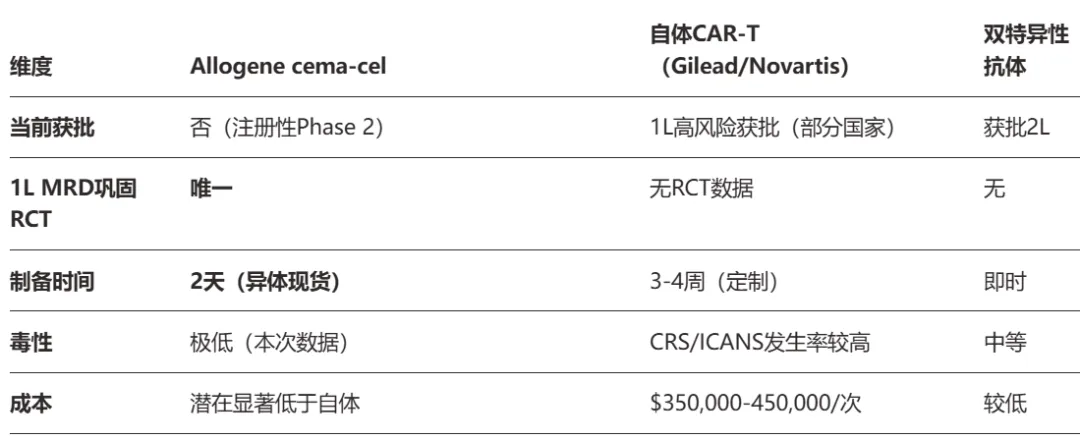
(Cema-cel的差异化和竞争定位)
大家可能好奇的是,中期无效性分析为何只有12例患者的数据?需要明确的是,中期无效性分析和中期疗效分析这两个概念其实有很大的不同。
无效性分析一般要证明的是"有没有明显迹象表明药不可能有效",所以它的设计触发的逻辑是“用最少的患者、在最早的时间点,判断这个试验是否值得继续投入资源”,Allogene的ALPHA3研究设计是“每组12例、合计24例患者都完成了随机分组后第45天的MRD检测”。
文献中LBCL MRD阳性患者在自然观察下的MRD自发转阴率约10-20%,而有临床意义的干预效果通常要求绝对差值≥25-30%,ALPHA3研究41.6%的绝对差值显著超过这一门槛(试验组患者基线更差),且ctDNA变化对比差异极大(ctDNA中位变化:试验组-97.7% vs 观察组+26.6%),数据将Cema-cel的成功率显著去风险化。
02
超干净的安全谱?
在这一次中期无效性分析中,真正超预期的应该是安全性。
这次Cema-cel的小样本分析数据,可能是目前为止所有CAR-T产品(自体或异体)安全性最干净的记录之一。
在已有的自体CAR-T(axi-cel、tisa-cel)1L研究数据:所有等级CRS发生率30-50%都算低的(有研究甚至高达100%),≥3级CRS和ICANS分别为5-15%、15-35%,几乎所有患者需要住院。
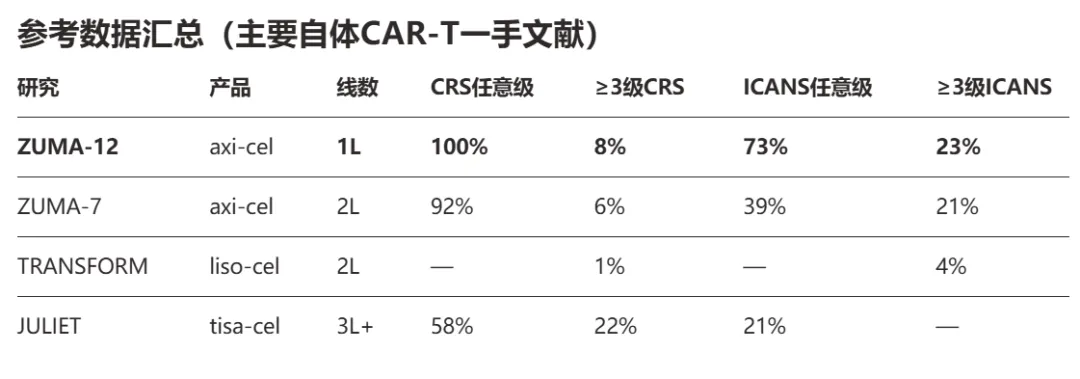
在Cema-cel的ALPHA3研究中,12例患者零CRS、零ICANS。在12例患者中,10例患者全程门诊给药,2例例短暂住院(不良事件均判定与Cema-cel无关)。如果未来这样的安全谱在更大样本中维持,将有望改变CAR-T治疗场景(全程门诊给药的可能性)。
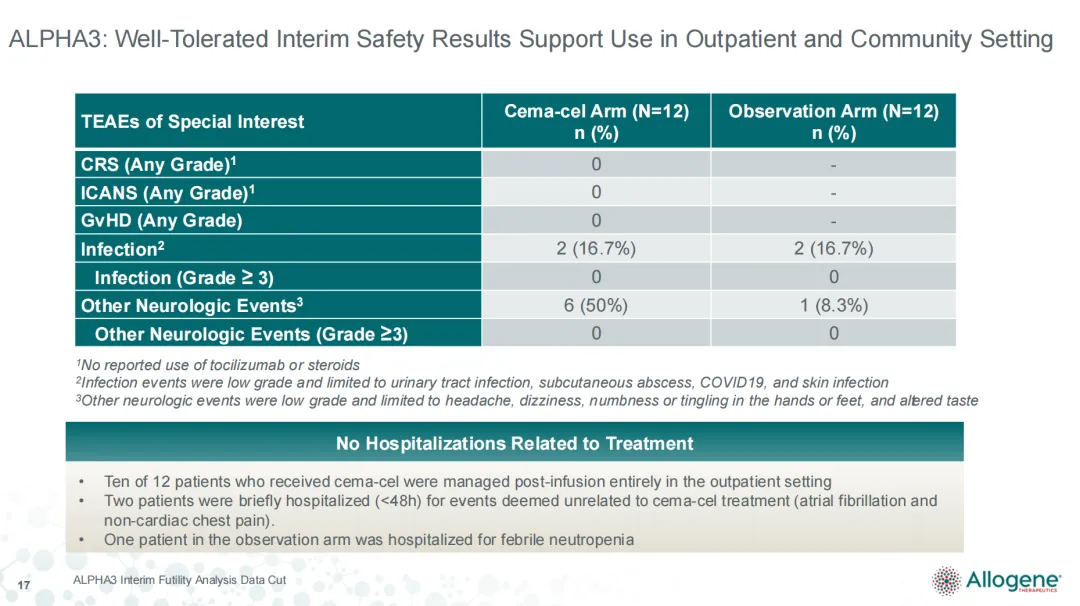
不过需要注意的是,由于适应症线数的不同,ALPHA3研究的安全性数据并不代表Cema-cel在后线患者中能够实现类似的表现,原因何在?
ALPHA3研究入组的是影像学CR、仅MRD阳性的低肿瘤负荷患者,例如ZUMA-12入组的是高危、PET阳性的活动性肿瘤患者。两者肿瘤负荷差异本身就会导致CRS/ICANS发生率不同——部分安全性差异来自适应症设计,而非单纯来自产品差异。
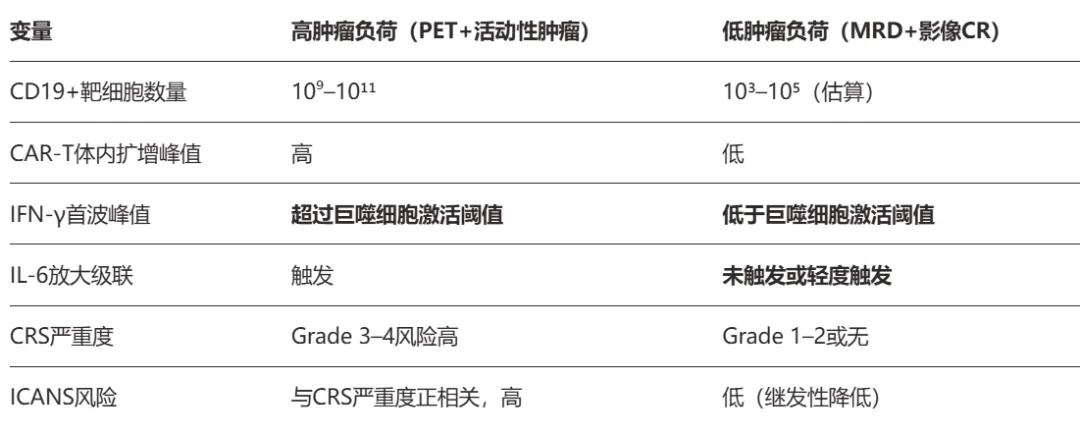
当然,不能仅以适应症入组群体差异否定Cema-cel的差异性,产品本身具备一定的设计差异化:1)公司使用TALEN技术敲除TCR和HLA,同时采用4-1BB共刺激域(相比采用CD28共刺激域的产品细胞因子释放更渐进、峰值更低,临床数据表明诱发的CRS发生率更低);2)异体CAR-T由于采用的是健康人T细胞,细胞因子释放更为可控;3)Cema-cel的清淋方案采用标准的“氟达拉滨+环磷酰胺”,这与公司过去其他产品采用CD52抗体清淋的效力更温和,在可能牺牲疗效的背景下降低CRS风险...

03
风险还没解除
Allogene还不能松一口气,Cema-cel未来要实现去风险化还有太多里程碑。
首先中期无效性分析仅仅代表“药物有没有疗效的可能性”,而这次读出数据的样本量足够小,那么疗效存在被小样本量患者放大的可能性。
要明确的是,ALPHA3研究设计共入组240例患者,主要终点是无事件生存期(EFS),次要终点是MRD转化率,研究EFS中期数据读出仍需要等待至2027年上半年,而MRD转阴到EFS改善的转化率仍具备不确定性,尽管有文献指出MRD持续阳性患者2年EFS约30-40%,MRD转阴患者约70-80%,小样本RCT数据预判全局仍有很大风险。
异体CAR-T在人体内的持续性是一个老生常谈的核心问题。
从已有数据人体内CAR-T的清除时间来看,ALLO-647在ALPHA/ALPHA2研究中大概是4个月左右存活时间,而预计ALPHA3研究由于清淋方案的改变,抗宿主免疫的压力更大,存活时间可能仅2–6周。

不过,从ALPHA/ALPHA2研究的反应持续时间和人体存活时间存在显著矛盾,CAR-T细胞在4个月内清除,但CR却维持23个月甚至4年以上。(有可能代表异体CAR-T在持续时间与疗效持久性的关联弱于自体CAR-T产品)

那么这样的矛盾性可能支持ALPHA3研究的正面推论,由于ALPHA/ALPHA2研究面向高肿瘤负荷患者,Cema-cel在ALPHA3研究的极低负荷场景中,即使持续时间更短(2–6周),也有机会足以消灭少量残留克隆并触发持久缓解。
当然,最终确定的结论还需要等到ALPHA3研究中期EFS分析的出炉。
结语:ALPHA3研究中期无效性分析的积极趋势,即是Allogene公司差异化选择适应症的结果,同时也给众多异体CAR-T的研发者打开了一扇差异化开发的大门,毕竟早线、肿瘤维持治疗是一个很大的市场,无论血液瘤和实体瘤均是。
或许渐渐地国内差异化路线异体CAR-T开发企业可以看起来了。

 研发追踪
研发追踪
 一度医药
一度医药  2026-04-20
2026-04-20
 107
107

 研发追踪
研发追踪
 一度医药
一度医药  2026-04-20
2026-04-20
 109
109

 研发追踪
研发追踪
 医药笔记
医药笔记  2026-04-20
2026-04-20
 105
105