 研发追踪
研发追踪
 谈思生物
谈思生物  2026-04-22
2026-04-22
 5
5
刚刚!世界首批 iPSC 疗法获批!!
诱导性多能干细胞疗法破冰:
日本率先商业化,科学界忧虑与期待并存
2026年3月,日本厚生劳动省相继批准两款 iPSC 来源的再生医学产品,分别靶向帕金森病与缺血性心肌病。这是人类首次将诱导多能干细胞技术推向临床商业化,但其背后的数据争议,或将深刻影响全球再生医学的监管走向。
来源 Nature Biotechnology 发布2026年4月17日 监管机构日本厚生劳动省
Nature Biotechnology
News in Brief

背景
2012年,山中伸弥因发现诱导多能干细胞(iPSC)技术荣获诺贝尔生理学或医学奖。彼时,科学界普遍预言这项技术将在十年内重塑再生医学的临床图景。然而现实的推进远比想象曲折——直至2026年3月6日,这一预言才以一种争议性的方式抵达终点。
日本厚生劳动省在同一天相继批准两款 iPSC 来源疗法的附条件限时上市许可(Conditional and Time-limited Marketing Approval),标志着人类历史上首批 iPSC 再生医学产品正式进入临床应用。这一时刻,在科学史上的重量毋庸置疑;然而伴随其后的争议与忧虑,同样不容忽视。

两款产品解析
此次获批的两款产品分别针对两种截然不同的适应症,代表了 iPSC 技术在中枢神经系统与心肌再生领域的并行探索。
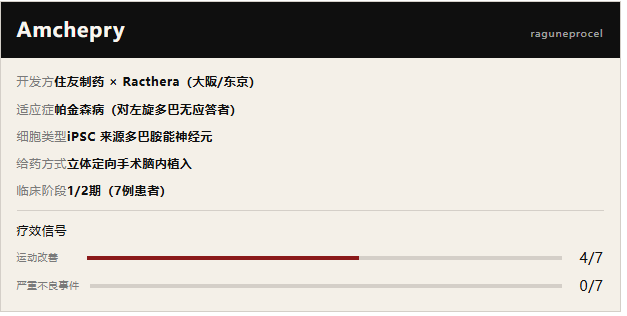
两项产品的技术路线值得深思。Amchepry 选择了细胞替代策略——将 iPSC
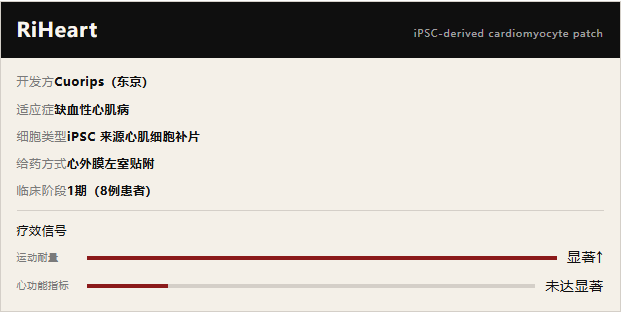
分化为多巴胺能神经元后立体定向植入纹状体,试图重建退变神经回路;RiHeart
则采用心肌补片模式,依赖旁分泌效应与结构支撑来改善心肌微环境,而非直接实现功能性电-机械整合。
技术注解
帕金森病的核心病理在于黑质致密部多巴胺能神经元的进行性凋亡,引发纹状体多巴胺信号缺失。现有药物疗法(左旋多巴)本质上是外源性多巴胺前体补充,随病程推进疗效衰减、运动并发症加剧。iPSC 来源多巴胺能神经元的植入,理论上可从根本上重建受损回路,而非依赖逐渐失效的化学替代。
RiHeart 所代表的心肌补片策略,其作用机制仍存争议。2025年1期结果显示运动耐量改善,但心功能关键指标(射血分数等)未见统计显著性改变,提示其治疗效果可能更多来自旁分泌信号调控而非真正的心肌再生。这一结论与 iPSC 来源心肌细胞的成熟度问题密切相关——体外分化的心肌细胞普遍停滞于胎儿样表型,电生理特性与成人心肌存在本质差异。
「我支持 iPS 细胞科学,但我质疑在证据不充分的情况下过早商业化。」
—— 河口浩(Hiroshi Kawaguchi),千叶那道谷医院骨科医生,接受《自然》采访时表示
争议焦点
在日本以外,科学界对上述批准普遍持保留态度。批评的核心并非技术本身,而是数据规模与监管逻辑之间的张力。
⚠ 科学界主要关切
样本量极为有限——两项试验合计15例患者,远不足以评估低频但严重的不良事件(如畸胎瘤形成、免疫排斥)的发生率
长期安全性数据缺失:iPSC 来源细胞的致瘤风险需要数年乃至十年以上的随访才能得到充分评估
长期免疫抑制方案尚不明确——异体来源细胞的宿主排斥反应管理策略缺乏大样本验证
疗效终点的临床意义存疑:RiHeart 的主要获益仅体现于运动耐量,而非心功能客观改善
「附条件限时上市」制度本身的边界:日本再生医学特别法允许更低证据门槛的条件批准,但商业化后的真实世界数据收集机制能否补足缺口,有待观察
日本监管生态
理解此次批准,必须置于日本独特的再生医学监管框架之中。2014年颁布的《再生医学安全确保法》及《药事法》修订案确立了"附条件、限时"批准通路,允许以早期临床数据换取阶段性上市许可,并要求企业在商业化过程中持续收集真实世界证据,以便在规定期限内申请完全批准或撤销。
2006
山中伸弥实验室发表 iPSC 技术,小鼠成纤维细胞重编程为多能状态
2012
山中伸弥荣获诺贝尔生理学或医学奖;人 iPSC 技术进入加速发展阶段
2014
高桥政代团队完成全球首例 iPSC 来源视网膜色素上皮细胞移植(自体)
2021
京都大学开展帕金森病 iPSC 神经元脑内移植 1期试验,住友制药参与产业化推进
2024
Aurion Biotech 的 Vyznova(neltependocel)获批,成为全球首个上市的角膜内皮细胞疗法
2026
Amchepry 与 RiHeart 获批,人类首批 iPSC 再生医学产品正式进入商业化应用
编辑观察
刚刚 BME · 深度视角
这两款产品的获批,在历史意义与现实隐忧之间划出了一道清晰的裂隙。历史层面,这是继人类胚胎干细胞疗法之后,多能干细胞首次在系统性再生医学层面实现临床商业化,为 iPSC 领域十余年的基础投入提供了第一个"概念成立"的监管注脚。
方法论层面,异体 iPSC 疗法的逻辑优势恰在于可规模化制备、建立细胞库,从而突破自体来源的成本与时间壁垒——这是 Amchepry 和 RiHeart 共同依赖的商业前提。然而这一优势本身也带来了长期免疫管理的新挑战,必须通过大样本长期随访加以厘清。
监管层面,日本的"附条件批准"路径正在成为全球再生医学监管创新的参照系。欧洲的 ATMP 条件批准、美国 FDA 的 RMAT 指定,均在探索类似的弹性框架。问题的核心在于:商业化压力是否会侵蚀真实世界证据的收集质量?日本迄今尚无一款依此路径获批的再生医学产品在规定期限内成功完成完全批准,这一前车之鉴值得警惕。
对于中国的骨科与心脏科同道而言,此次日本的监管动向提供了重要的参照维度。国家药品监督管理局(NMPA)目前尚未建立对标的 iPSC 疗法快速通道,但随着本土 iPSC 心肌、软骨、角膜等适应症项目相继进入临床,相关政策窗口或将在近年内开启。

 研发追踪
研发追踪
 医药观澜
医药观澜  2026-04-22
2026-04-22
 5
5

 研发追踪
研发追踪
 药闻天下
药闻天下  2026-04-22
2026-04-22
 4
4

 研发追踪
研发追踪
 药事纵横
药事纵横  2026-04-22
2026-04-22
 5
5
 热门资讯
热门资讯