 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-04-25
2026-04-25
 39
39
恒瑞的 GLP-1 野心,已从产品竞争延伸到全球市场。
2026 年 4 月,恒瑞的 NewCo 公司 Kailera 连续完成两步关键动作:4 月 13 日启动 IPO,4 月 16 日成功在纳斯达克挂牌上市,募资总额约 6.25 亿美元。至此,这家成立不足两年的美国 Biotech 公司,凭借从恒瑞引进的 GLP-1产品组合,已经完成 10 亿美元融资,并将双靶点减重资产瑞普泊肽推进至全球 III 期阶段。
Kailera 的上市,把恒瑞 GLP-1 布局的分量一下子抬了出来。通过 NewCo,恒瑞把 GLP-1 资产后期全球开发最烧钱的阶段交给外部资金承接,海外市场一旦跑通,股权、里程碑和后续收入都留有空间,这也是恒瑞连接全球市场的一块关键跳板。
把牌面铺满
恒瑞试图把 GLP-1 做成一个长期经营的代谢平台,其 GLP-1 台面上已经摆出四条线,注射版和口服版瑞普泊肽(Ribupatide;HRS-9531)、HRS-7535(KAI-7535)以及 HRS-4729(KAI-7535)。这四条管线覆盖了注射、口服两种剂型,双靶点、三靶点两代机制,大分子、小分子两种技术路径。管线组合布局极具差异化,放在国内同赛道里,能同时拥有多个维度布局的公司屈指可数。
其中,走得最快的是瑞普泊肽。作为恒瑞自研的 GLP-1/GIP 双靶点激动剂,瑞普泊肽与礼来替尔泊肽同机制,也是恒瑞手里最接近兑现的一张牌。它在中国已经走完 II 期和 III 期临床,数据本身也足够撑起市场预期。
注射剂型中国 III 期减重研究积极顶线结果显示,在为期 48 周的试验中,6 mg 剂量组平均减重 19.2%,安全性良好且未达平台期;8 mg 的中国 II 期减重研究中,36 周后,瑞普泊肽治疗组平均体重较基线下降 23.6%,安全性和耐受性同样良好。这个临床试验结果,在非头对头对比的情况下,效果已和替尔泊肽不相上下。
此外,口服剂型也已经跑出数据。2026 年 2 月披露的中国 Ⅱ 期减重研究积极顶线结果显示,治疗第 26 周时,瑞普泊肽治疗组较基线平均体重下降最高达 12.1%,且未观察到平台期,呕吐发生率不超过 11.4%。
当前,瑞普泊肽注射剂型用于成人长期体重管理的上市申请已获得中国 NMPA 受理,口服剂型计划在中国推进肥胖症 Ⅲ 期临床,拟开发适应症覆盖超重/肥胖及相关合并症、2 型糖尿病。
全球开发节奏也在加快。2026 年 1 月,Kailera 已启动瑞普泊肽注射剂型的全球 Ⅲ 期 KaiNETIC 项目,其中 KaiNETIC-3 直接头对头对比诺和诺德的 Wegovy;另外,口服剂型也最早有望于 2027 年上半年启动全球 Ⅲ 期。
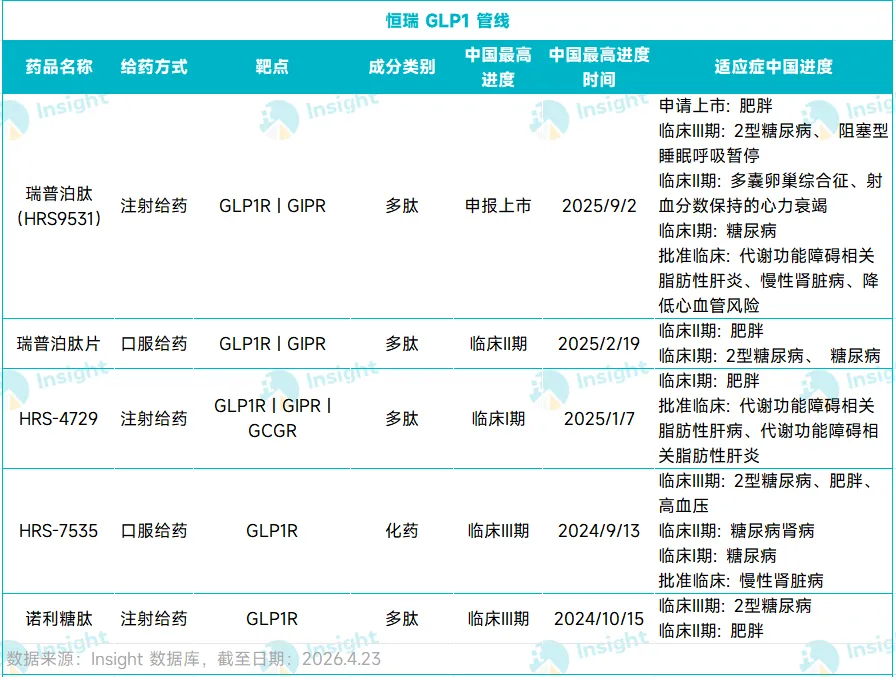
HRS-7535 和 HRS-4729 对应恒瑞的另外两步棋。
HRS-7535 是一款新型口服小分子 GLP-1R 激动剂。目前,全球范围内仅一款口服小分子 GLP-1R 激动剂 Orforglipron 获批上市,还有 3 款处于 III 期临床阶段,HRS-7535 是其中之一。
HRS-7535 针对超重/肥胖、2 型糖尿病都已推进至 Ⅲ 期,预计 2026 年读出数据。2026 年 1 月,NMPA 又批准了 HRS-7535 用于高血压合并超重/肥胖的新适应症临床试验,场景进一步扩到代谢共病管理;今年,HRS-7535 还将启动全球 Ⅱ 期临床。
HRS-4729 则是更前沿的管线储备。作为 GLP-1/GIP/GCG 三靶点激动剂,与双靶点相比,增加 GCG 靶点激活后,可促进能量消耗、降低血脂,更好地发挥减重效果。该药已于 2024 年 12 月获批开展超重/肥胖适应症临床试验,目前正在中国进行 Ⅰ 期临床,Kailera 也计划于今年启动全球Ⅰ期临床,全球范围内尚无同类产品上市。
综合来看,双靶点注射和口服产品瑞普泊肽卡住当前最成熟的市场机会,口服小分子 HRS-7535 和三靶点资产 HRS-4729 则为后续产品迭代留出余地。放到 GLP-1 竞争格局里,恒瑞打出了四张很硬的产品牌。
抢全球市场
恒瑞在 GLP-1 上的野心,并没有停留在产品层面,市场端同样提前展开。
2024 年 5 月,恒瑞医药以 NewCo 模式,将 4 款 GLP-1 核心资产大中华区以外的全球开发、生产和商业化权利独家授权给 Kailera。按照协议,恒瑞获得 1.1 亿美元首付款、累计不超过 2 亿美元的临床开发及监管里程碑款、以及累计不超过 57.25 亿美元的销售里程碑款,时持有 Kailera 19.9% 股权(IPO 后稀释至 13.6%)。
合作之后,恒瑞和 Kailera 共同努力,稳步推进 GLP-1 产品组合在海内外的开发落地,恒瑞负责大中华区,Kailera 负责大中华区以外地区。这笔交易之后,恒瑞的这批 GLP-1 资产开始直接面向全球市场推进。
放在近两年中国 GLP-1 资产出海潮里看,恒瑞与 Kailera 这笔交易很有代表性。
2024 年 12 月,翰森将口服小分子 GLP-1 HS-10535 以 20.12 亿美元总价授权默沙东,HS-10535 也成为中国首个出海的口服 GLP-1 类药物;
2025 年 3 月,联邦制药把 GLP-1/GIP/GCG 三靶点受体激动剂 UBT251 以 20 亿美元总价授权给诺和诺德;
2025 年 6 月,翰森又将 GLP-1/GIP 双受体激动剂 HS-20094 的海外权益授予再生元,拿到 8000 万美元首付款和最高 19.3 亿美元潜在里程碑付款;
2025 年 12 月,辉瑞与复星医药旗下的药友制药达成全球独家合作,引进口服小分子 GLP-1 受体激动剂 YP05002,潜在总交易金额高达 20.85 亿美元。
2026 年 1 月,阿斯利康与石药集团达成一项总对价高达 185 亿美元的合作,合作内容包括获得石药集团每月一次注射用体重管理产品组合的全球独家权利,包括长效 GLP1R/GIPR 激动剂 SYH2082;
2026 年 2 月,辉瑞又以 4.95 亿美元引入先为达的埃诺格鲁肽在中国大陆的独家商业化权益。
MNC 在扫货,中国公司也在集中兑现。在这些交易里,恒瑞这笔 NewCo 和传统 license-out 的差别很明显。石药、翰森、联邦的交易,核心都是把海外权益交给 MNC,后续全球开发节奏、商业化路径和市场定价,基本都由对方主导。
恒瑞通过 NewCo,把 4 款 GLP-1 资产被整体装进 Kailera,恒瑞手里除了首付款、里程碑和未来销售分成,还保留了一层股权价值。Kailera 一旦在美股获得更高估值,恒瑞可以直接分享 GLP-1 赛道的流动性溢价。瑞普泊肽一旦在美国获批,恒瑞拿到的也不只是一次性 BD 收入,后面还有持续的里程碑和现金流回报。这种打法,在当前中国 GLP-1 出海案例里极具代表性。
打开资本空间
产品和市场之外,真正拉开层次还在资本端。4 月 13 日,Kailera 正式向美国 SEC 递交招股书,启动 IPO,计划发行 3333.33 万股,发行价区间为每股 14 美元至 16 美元,并拟以「KLRA」为代码在纳斯达克挂牌上市。
据 Kailera 招股文件显示,Kailera 成立后不久便与恒瑞签署授权协议,取得恒瑞旗下的 HRS-7535、HRS9531、HRS-4729 等在研管线在大中华区以外的权益。
协议签订后,Kailera 迅速完成资本布局,2024 年 10 月完成 4 亿美元 A 轮融资,贝恩资本、RTW Investments 等机构入局;2025 年 10 月再完成 6 亿美元 B 轮融资,位列当年全球制药领域融资第二。资金到位后,Kailera 在 2025 年底至 2026 年初启动 KaiNETIC 全球 III 期临床,总样本量超过 4700 人。
2026 年 4 月 16 日,Kailera 成功在纳斯达克挂牌上市,本次发行预计募资总额为 6.25 亿美元,且该金额不包括承销商行使超额配售权购买额外股份。
Kailera 成功上市,对恒瑞具有现实意义,恒瑞持有的 13.6% 股权(上市后稀释至 9.8%)将进入公开市场估值体系,同时最高约 59.25 亿美元的里程碑付款也将逐步兑现。首付款和里程碑带来的确定性收入,已经足以覆盖相关管线在国内的早期研发投入,此外还有未来非常具备弹性的全球收入预期。
站在恒瑞自身的视角来看,这是一种很务实的安排,后期全球临床的高投入部分被拆分出去,海外市场又没有完全交掉。海外市场一旦跑出来,收益极其可观。
此外,恒瑞 2025 年年报已经显示了出海战略的兑现速度。全年营收 316.29 亿元,同比增长 13%,创新药收入 163.42 亿元,首次超过药品销售总额的 50%。技术许可和相关收入达到 33.92 亿元,同比增长 25.6%。再加上 2025 年 5 月完成的港股上市,募资约 112 亿港元,恒瑞的国际资本通道也进一步打通。
放在恒瑞庞大的整体管线里,GLP-1 不仅是代谢领域的核心资产之一,还是恒瑞连接全球市场的一块关键跳板。恒瑞正向全球化创新药企阔步迈进!
结语
当然,野心越大,约束也越现实。美国肥胖药市场的竞争门槛很高,礼来与诺和诺德在产能、渠道覆盖以及医生端认知上已经占住先发优势,监管与市场资源也在持续向头部集中。
与此同时,国内市场同样不轻松。司美格鲁肽在中国的核心专利已到期,国内多款仿制药蓄势待发,价格战已经开始铺开。内外承压,恒瑞在未来在 GLP-1 邻域能够拿到什么结果,仍需要继续观察。

 研发追踪
研发追踪
 罕见病信息网
罕见病信息网  2026-04-27
2026-04-27
 48
48

 研发追踪
研发追踪
 Medaverse
Medaverse  2026-04-27
2026-04-27
 47
47

 研发追踪
研发追踪
 药明康德
药明康德  2026-04-27
2026-04-27
 48
48
 热门资讯
热门资讯