 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-04-23
2026-04-23
 10
10
2026 年 AACR 于 4 月 17 日至 22 日在美国加利福尼亚州圣地亚哥盛大召开。随着国内创新药企业在全球竞争力的显著提升,多款国产新药携临床数据亮相本次大会。
Insight 数据库从中梳理了 10 款首次披露相关临床数据的国产创新药(不分先后),一览中国肿瘤创新的最新突破,供读者参考。*文首扫描二维码可获取 2026 年 AACR 摘要全量数据。
恒瑞医药
阿得贝利单抗联合化疗围手术期治疗 NSCLC 的 III 期临床
恒瑞在本次大会上以口头报告的形式首次公布阿得贝利单抗(研发代号:SHR-1316)联合含铂化疗作为可切除的 II-IIIB 期 NSCLC 患者围手术期治疗的 III 期研究结果。

截图来源:AACR 官网
该研究共入组 501 例受试者,按照 1:1 随机入组,分别接受 3 个周期阿得贝利单抗或安慰剂联合铂类双药化疗(Q3W),随后进行手术,术后接受 16 个周期的阿得贝利单抗或安慰剂辅助治疗。
数据截止时,中位随访时间为 23.6 个月。围手术期阿得贝利单抗联合化疗显著改善了无事件生存期(EFS)和主要病理缓解(MPR)率,另外,阿得贝利单抗联合化疗组的根治性手术率(88.8% vs 83.2%)和病理学完全缓解(pCR)率(31.1% vs 7.6%)也显著高于安慰剂组。
安全性方面,阿得贝利单抗联合化疗组和安慰剂组与任何研究药物相关的 ≥3 级不良事件发生率分别是 52.6% 和 53.6%;其中,阿得贝利单抗联合化疗组发生率 ≥2% 的所有不良事件均为血液学不良事件。
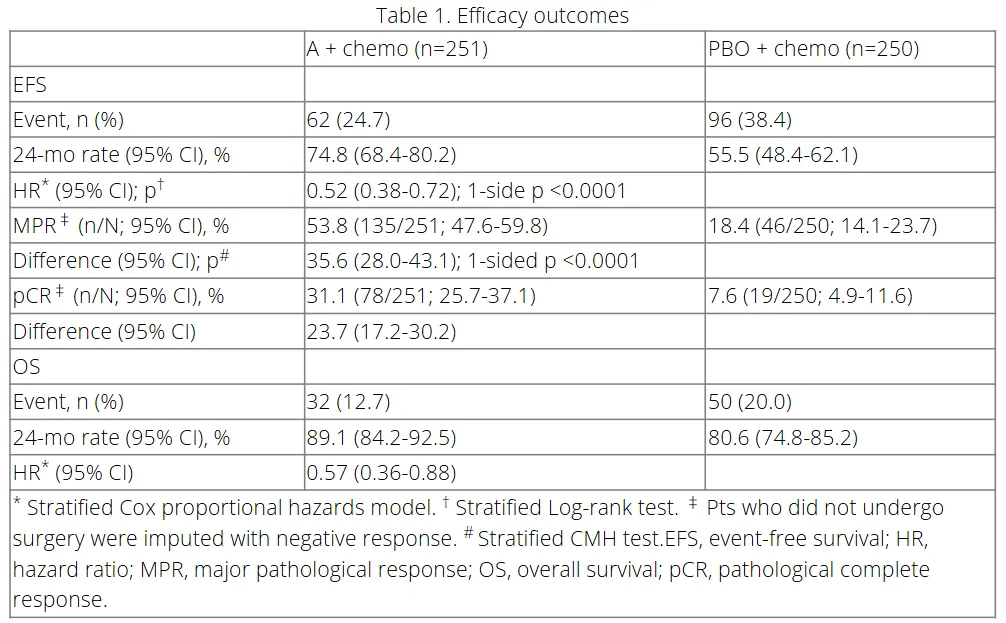
截图来源:AACR 官网
值得一提的是,基于该临床的积极结果,2025 年 9 月,CDE 已经受理了阿得贝利单抗新适应症的上市申请,适应症为:阿得贝利单抗联合含铂化疗作为新辅助治疗,术后继续以该药作为单药辅助治疗,用于治疗可手术切除的 II、IIIA 和 IIIB 期且无已知 EGFR 突变或 ALK 重排的成人 NSCLC 患者。
百济神州
替雷利珠单抗联合用药一线治疗头颈鳞癌的 II 期临床
百济神州在本次大会上以口头报告的形式首次公布一项 II 期、开放标签、国际性研究的结果,该研究评估了替雷利珠单抗联合或不联合 TIM-3 单抗 Surzebiclimab(SUR)和/或 LAG-3 单抗 Alcestobart(LBL-007)作为一线治疗方案在复发/转移性 HNSCC 患者中的疗效 (NCT05909904)。

截图来源:AACR 官网
该研究纳入符合条件的患者为年龄≥18 岁,经组织学/细胞学确诊为复发/转移性头颈部鳞状细胞癌(R/M HNSCC),且 PD-L1 表达阳性(CPS 评分≥1)。患者随机分组,分别接受替雷利珠单抗单药治疗(A 组)、替雷利珠单抗联合 SUR 治疗(B 组)、替雷利珠单抗联合 LBL-007 治疗(C 组)或替雷利珠单抗联合 SUR 和 LBL-007 治疗(D 组)。
截至 2025 年 6 月 17 日,共入组 160 例患者(每组 40 例)。研究的中位随访时间为 13.1 个月。各治疗组的 ORR 相似,A、B 和 D 组的确认 ORR 为 27.5%,C 组为 25.0%。 C 组 3 例患者和 D 组 2 例患者达到完全缓解。A 组临床获益率为 32.5%,B 组和 D 组为 37.5%,C 组为 35.0%。A 组、B 组、C 组和 D 组的 DCR 分别为 55.0%、67.5%、62.5% 和 65.0%。
各组的治疗耐受性良好,毒性反应可控。在所有患者中,最常见的 TEAE 为贫血、甲状腺功能减退和天冬氨酸氨基转移酶升高。A、B、C 和 D 组分别有 67.5%、61.5%、77.5% 和 67.5% 的患者发生与治疗相关的 TEAE。
在所有患者中,5.7% 的患者发生致命性 TEAE,其中无一例与治疗相关。在所有患者中,35.2% 的患者发生免疫介导的不良事件;大多数为 1 级或 2 级,且不严重。在所有患者中,6.9% 的患者发生输注相关反应,A 组仅报告 1 例 ≥3 级事件。
研究者得出结论,对于 R/M HNSCC 患者,在替雷利珠单抗作为一线治疗方案中加入 SUR、LBL-007 或 SUR 和 LBL-007 并无额外获益。
翰森制药
HS-10504 治疗 EGFR 突变阳性 NSCLC 的首次人体研究
EGFR C797S 突变是三代 EGFR TKIs 治疗 EGFR 突变 NSCLC 后的主要耐药机制,目前尚无经过临床验证和可用的靶向治疗药物。HS-10504 是一种新型、高效且高选择性四代 EGFR-TKI,旨在靶向 EGFR 敏感突变和 C797S 突变(伴或不伴 T790M 突变)而设计。

截图来源:AACR 官网
在本次大会上,翰森制药公布了 HS-10504 的首次人体 I 期研究初步结果。截至 2025 年 12 月 25 日,82 例患者入组并接受治疗。剂量递增阶段(n=20)未观察到剂量限制性毒性,且在剂量 500 mg QD 时未达到最大耐受剂量。剂量扩展阶段进一步研究了 300 mg 和 400 mg QD,400 mg 剂量下的 HS-10504 治疗具有更佳的临床获益。
在接受 400 mg QD 剂量治疗的患者(n=35)中,所有患者为 Ⅳ 期腺癌,具有 EGFR C797S 突变。25 例患者(71.4%)既往接受过 ≥2 线抗肿瘤治疗,所有患者均接受过至少 1 种三代 EGFR-TKI 治疗。
结果显示,34 例疗效可评估的患者具有令人鼓舞的抗肿瘤活性。17 例(50%)患者部分缓解,14 例(41.2%)病情稳定。cORR 为 47.1%,DCR 为 91.2%。截至数据截止日期,大多数患者仍在接受治疗。
总体而言,HS-10504 显示出良好且可控的安全性,大多数 TEAEs 为 1-2 级。≥3 级 TEAEs 发生率为 74.3%(26/35),主要为实验室检查异常,包括淋巴细胞减少和贫血,这些不良事件均可临床控制。导致永久停药的 TEAEs 发生率为 2.9%(1/35),未报告致死性 TEAEs。
康方生物
卡度尼利联合疗法一线治疗胰腺癌的 II 期临床
尽管免疫治疗在多种实体瘤中展现出显著疗效,但因胰腺癌固有的免疫逃逸特性及高度抑制的肿瘤微环境,全球范围内既往免疫疗法针对转移性胰腺癌一线治疗的 III 期研究均未取得突破,迄今也尚无免疫治疗方案获批。
COMPASSION-26 是康方生物启动的一项多中心、开放性、II 期临床研究,旨在评价 PD-1/CTLA-4 双特异性抗体卡度尼利单抗(研发代号:AK104)联合化疗一线治疗不可手术切除的局部晚期或转移性胰腺癌的疗效和安全性。

截图来源:AACR 官网
截至 2025 年 10 月 20 日,共纳入 59 例既往未接受过全身治疗的不可切除的晚期或转移性胰腺导管腺癌(PDAC)患者,中位随访 24.7 个月,数据显示:
卡度尼利联合方案带来良好的生存获益,在局晚期患者的生存获益更为突出:全人群 mOS 为 13.8 个月;局晚期患者的 mPFS 为 11.1 个月,mOS 为 23.4 个月,12 个月生存率达 91.7%,24 个月生存率达 44.1%。
卡度尼利联合方案具有良好的肿瘤控制能力,56 例患者(95%)的患者完成了至少一次基线后肿瘤评估,ORR 为 33.9%,DCR 达 96.4%;局晚期与转移性患者的缓解率无显著差异,均能从卡度尼利联合方案中获益。
所有患者均发生治疗相关不良事件(TRAE),最常见的不良事件包括中性粒细胞计数降低、贫血、白细胞计数降低、血小板计数降低、皮疹、丙氨酸氨基转移酶升高、天冬氨酸氨基转移酶升高、脱发、淋巴细胞计数降低、发热、乏力和瘙痒。未发现新的安全性信号。
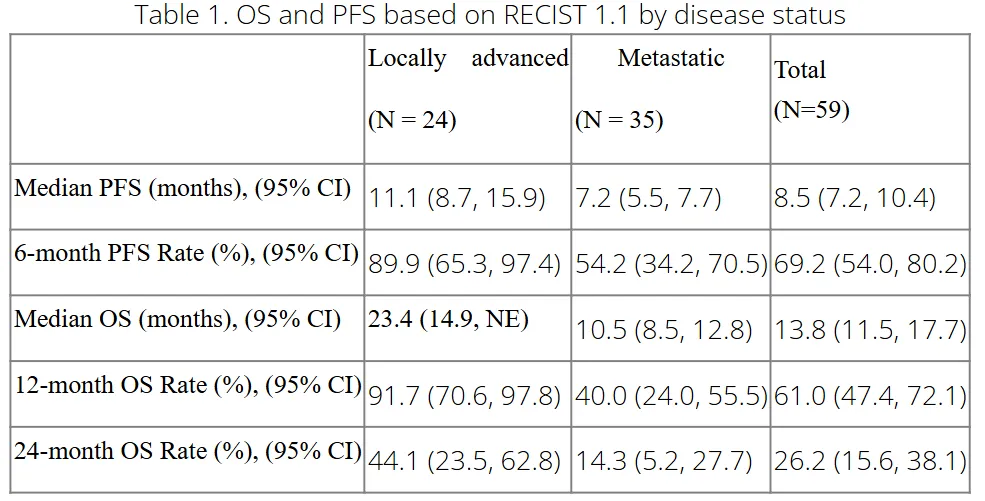
截图来源:AACR 官网
齐鲁制药
QLS5132 用于治疗铂类耐药卵巢癌的 I 期临床
QLS5132 是齐鲁制药自主研发的一款靶向 CLDN6 的 ADC 药物,兼具传统小分子细胞毒药物的强大杀伤效应和抗体药物的精准靶向性。

截图来源:AACR 官网
I 期临床(NCT06932094)数据显示,截至 2026 年 1 月 21 日,共纳入 28 名晚期铂类耐药卵巢癌患者,其中卵巢癌 26 例,输卵管癌 2 例。疗效方面,其中 9 例受试者达到部分缓解 (PR)(3.2 mg/kg 剂量组 2 例,4.8 mg/kg 剂量组 5 例,6.4 mg/kg 剂量组 2 例)。
在所有剂量组的 18 例疗效可评估患者中,ORR 和 DCR 分别为 50.0% 和 94.4%,在 ≥3.2 mg/kg 剂量组的 17 例疗效可评估患者中,ORR 和 DCR 分别为 52.9% 和 100%。
安全性方面,6.4 mg/kg 剂量组 1 例患者出现 4 级血小板计数下降的剂量限制性毒性。26 例(92.9%)患者出现 TEAE(92.9% 与治疗相关)。发生率超过 50% 的最常见 TRAE 包括恶心、厌食、贫血和乏力。脱发、骨痛、背痛、感觉减退和口腔黏膜炎分别发生于 1 例(3.6%)患者。未发生间质性肺病、眼毒性或发热性中性粒细胞减少症。大多数胃肠道不良反应为 1 级或 2 级。
9 例(32.1%)患者发生≥3 级不良反应。≥3 级血液学不良反应在 6.4 mg/kg 剂量组 2 例(66.7%)患者中发生,在<6.4 mg/kg 剂量组 5 例(20.0%)患者中发生。1 例(3.6%)6.4 mg/kg 剂量组患者发生治疗相关不良反应(TRSAE),均为血液学毒性。未发生导致治疗中断或死亡的 TRAE。
翰森制药
HS-20093 联合阿得贝利单抗治疗驱动基因阴性的非鳞状 NSCLC 的 I 期临床
HS-20093(Risvutatug rezetecan)是一款 B7-H3 ADC,2023 年 12 月,翰森制药授予 GSK 关于该药的全球独家许可(不包含中国内地及港澳台),以开发、生产和商业化该产品。目前该产品正由 GSK 在海外推荐临床 I 期及 III 期临床试验。
ARTEMIS-101 是一项开放标签、多中心的 I 期研究,旨在评估 HS-20093 联合其他抗肿瘤药物在晚期实体瘤患者中的安全性、有效性、药代动力学和免疫原性,包括 5 个队列。其中队列 1 中,患者接受 HS-20093 8.0 mg/kg 和阿得贝利单抗 20.0 mg/kg 每三周一次静脉注射,直至出现疾病进展或不可耐受毒性。

截图来源:AACR 官网
在本次 AACR 大会上,翰森制药以口头报告形式首次公布了 ARTEMIS-101 研究队列 1 中的一个亚组(既往经治的驱动基因阴性的非鳞 NSCLC)数据。
截至 2025 年 10 月 20 日,共有 40 例患者入组并接受 ≥1 剂治疗,中位随访时间 8.7 个月。所有患者接受过 ≥1 线系统抗肿瘤治疗:含铂化疗(100%),免疫治疗(75.0%)和抗血管生成药物(45.0%)。
34 例疗效评估患者中,cORR 为 47.1%,DCR 为 94.1%。中位 DoR 为 12.6 个月,中位 PFS 为 14.0 个月(32.4% 事件发生率),OS 数据仍未成熟。
在既往接受过化疗和免疫治疗而未接受过 TOP1i 治疗的患者中观察到类似疗效,cORR 为 52.2%。在所有 PD-L1 亚组中均显示出抗肿瘤活性:肿瘤比例评分(TPS)<1 的患者 cORR 为 33.3%,mPFS 11.2 个月;TPS≥1 的患者 cORR 62.5%,mPFS 数据尚不成熟。
HS-20093 联合阿得贝利单抗的整体安全性可控,TEAEs 导致的减量率和停药率分别是 20.0% 和 7.5%,无导致死亡的 TEAEs 发生。发生率 ≥20% 的 ≥3 级 TEAEs 包括白细胞计数降低、中性粒细胞计数降低、淋巴细胞计数降低和贫血。
值得一提的是,基于 ARTEMIS-101 研究结果,HS-20093 联合阿得贝利单抗获 NMPA 批准纳入突破性治疗药物,拟定适应症为既往经过含铂化疗后进展或复发的驱动基因阴性的局部晚期或转移性非鳞状非小细胞肺癌。
此外,基于初步安全性和疗效结果,翰森已经启动了一项该联合治疗针对既往经治的 AGAs 阴性 nsq-NSCLC 患者的一项 III 期临床研究(登记号:CTR20260641/NCT07464327)。
君实生物
JS212 首次人体临床研究
在本次 AACR 年会上,君实生物公布了 JS212 的首次人体临床研究初步结果,成为全球第二款公布临床研究结果的 EGFR/HER3 双抗 ADC。

截图来源:AACR 官网
JS212 的 I/II 期人体临床研究旨在评估 JS212 在晚期实体瘤患者中的安全性、耐受性、药代动力学特征和初步疗效,研究包括剂量递增与扩展(I 期)以及临床扩展阶段(II 期)。
截至 2026 年 3 月 26 日,研究共入组 63 例患者,均采用每 3 周给一次的给药方法。整体耐受性良好,最大耐受剂量(MTD)未达到。
在≥1.8 mg/kg 剂量组中,均观察到肿瘤缓解;4.2 mg/kg 和 4.6 mg/kg 剂量组的 ORR 分别高达 44.4% 和 50.0%,DCR 均为 100.0%,中位 DoR 尚未达到。在 HER2- 乳腺癌和食管鳞癌患者中的 ORR 分别达 50.0% 和 38.9%。
结果表明,JS212 单药治疗晚期实体瘤,在多个剂量水平(即使低至 1.8 mg/kg)中均显示出令人鼓舞的抗肿瘤活性,且耐受性良好,展示了良好开发潜力。
中国生物制药/默沙东
MK-2010 首次人体研究
MK-2010(LM-299)是中国生物制药子公司礼新医药研发的一款四价双抗,同时靶向 PD1 和 VEGF,其采用 IgG-VHH 融合结构并具有 Fcγ 沉默功能。2024 年 11 月,默沙东引进了该产品全球开发、生产和商业化权益,总金额高达 32.88 亿美元。
在本次会议上,默沙东公布了 MK-2010的首次人体研究的初步结果(登记号:NCT06650566)。
截图来源:AACR 官网
研究共有 112 例患者接受治疗,包括剂量递增队列(n=40)和非小细胞肺癌(NSCLC) 扩展队列(n=72)。扩展队列中包含重度经治患者(68% 有既往系统治疗史,60% 既往接受过抗 PD-(L)1 治疗,26% 既往接受过抗 VEGF 治疗)。剂量递增队列的中位随访时间为 7.9 个月,扩展队列的中位随访时间为 3.3 个月。治疗持续时间中位数分别为 2.6 个月和 2.1 个月。
结果显示,MK-2010 表现出可控的安全性特征,未观察到 5 级治疗相关不良事件(TRAEs),1 例因 TRAE 导致停药(发生于剂量递增队列)。NSCLC 扩展队列中,TRAEs 多为低级别,3-4 级 TRAEs 发生率低(17-27%),未报告治疗相关死亡;VEGF 抑制剂相关毒性可控,且绝大多数为≤3 级。
同时,已经观察到初步的抗肿瘤活性,在 NSCLC 扩展队列的初治患者中,20 mg/kg Q3W 组和 30 mg/kg Q3W 组的未确认客观缓解率(ORR)分别为 55% 和 44%。
海思科
HSK46575 用于转移性去势抵抗性前列腺癌的 I 期临床
CYP11A1 是类固醇生物合成的关键酶,是治疗去势抵抗前列腺癌(CRPC)耐药性和难治性的理想治疗靶点。HSK46575 作为新一代 CYP11A1 抑制剂,能够强效抑制类固醇激素及其前体的生成。
本次大会上,海思科首次公布了 HSK46575 用于转移性 CRPC 的 I 期临床初步结果。

截图来源:AACR 官网
截至 2025 年 10 月 27 日,共有 27 例患者接受了 HSK46575 治疗。在所有剂量递增队列中,AR 野生型或 AR 突变型患者的 PSA50 应答率为 30.8%(8/26)。其中,AR 突变型患者的 PSA 应答率更高。
HSK46575 在剂量递增期间表现出良好的临床安全性,TRAE 发生率为 63.0%,其中仅有 7.4% 的患者出现≥3 级 TRAE(截至 2025 年 9 月 9 日),且未发生剂量限制性毒性或治疗相关死亡。
研究者认为,该研究结果支持进一步开发 HSK46575 用于前列腺癌的临床治疗,包括单药治疗和合理联合用药。
君实生物
JS207 一线肝细胞癌、结直肠癌的两项 II 期临床
在本次 AACR 年会上,君实生物首次公布了 JS207 的两项 II 期临床结果。
一项是 JS207 联合 JS007 一线治疗晚期肝细胞癌(HCC)的 II 期研究初步结果,这也是首个报告抗 PD-1/VEGF 双抗联合抗 CTLA-4 疗法在晚期肝癌一线治疗取得积极临床获益的研究。

截图来源:AACR 官网
截至 2026 年 3 月 20 日,共 26 例患者接受了 JS207 联合 JS007(3 mg/kg Q6W 治疗 2 周期,之后 1 mg/kg Q6W,即推荐剂量)治疗,包括安全导入期 7 例,随机扩展阶段 19 例。
在 22 例疗效可评估患者中,联合治疗的 ORR 达 45.5%,DCR 达 86.4%;耐受性良好,安全导入期未观察到剂量限制性毒性(DLT)。
该研究初步结果表明,JS207 联合 JS007 在晚期 HCC 一线治疗中显示出令人鼓舞的抗肿瘤活性与良好的耐受性,为抗 PD-1/VEGF 联合抗 CTLA-4 的「双免疫+抗血管」三靶协同增效策略提供了强有力的初步证据。
另一项是 JS207 联合化疗一线治疗微卫星稳定或错配修复完整(MSS/pMMR)型转移性结直肠癌(mCRC)的 II 期临床研究。

截图来源:AACR 官网
这项开放、单臂、II 期临床研究(NCT06885385),计划纳入既往未接受过任何系统性抗肿瘤治疗,或在完成新辅助/辅助治疗至少 12 个月后出现疾病复发或进展的 MSS/pMMR 型 mCRC 患者,接受 JS207(10 mg/kg)联合 XELOX(奥沙利铂 130 mg/m2,d1+卡培他滨 1000 mg/m2,BID,d1-14)治疗,每 3 周给药一次,直至疾病进展或出现不可耐受的毒性。
截至 2026 年 1 月 13 日,共有 32 例患者入组并接受治疗,其中安全导入期 9 例和剂量扩展期 23 例。在 31 例疗效可评估患者中,22 例达到部分缓解(PR),8 例达到疾病稳定(SD),ORR 达 71.0%,DCR 为 96.8%。
由于随访时间尚短,中位 PFS 和中位 DoR 尚未成熟,最长缓解持续时间达 8 个月,且仍在持续。安全性方面,整体耐受性良好,安全导入期未观察到 DLT。
研究表明,JS207 联合化疗在 MSS/pMMR 型 mCRC 一线治疗中展现出积极的抗肿瘤作用和良好的安全性。该研究提示抗 PD-1/VEGF 双抗联合化疗在「免疫冷肿瘤」人群中具有良好的应用前景,为 MSS/pMMR 型 mCRC 的一线免疫联合治疗提供了重要的临床依据。
 研发追踪
研发追踪
 丁香园Insight数据库
丁香园Insight数据库  2026-04-23
2026-04-23
 10
10

 研发追踪
研发追踪
 医药观澜
医药观澜  2026-04-22
2026-04-22
 75
75

 研发追踪
研发追踪
 药闻天下
药闻天下  2026-04-22
2026-04-22
 77
77
 热门资讯
热门资讯