 产业资讯
产业资讯
 佰傲谷BioValley
佰傲谷BioValley  2026-05-14
2026-05-14
 442
442
日前,Kyverna Therapeutics已正式开始向FDA滚动提交其CAR-T细胞药物mivocabtagene autoleucel(miv-cel,研发代码:KYV-101)的生物制品许可申请,用于治疗僵人综合征(SPS)。
值得注意的是,这是首个提交上市申请的自免CAR-T。如果miv-cel顺利上市,将为CAR-T细胞治疗开辟更广泛的商业应用领域。
首个提交BLA的自免CAR-T
miv-cel是一款自体CD19 CAR-T细胞治疗,是最早进入临床的自免CAR-T产品之一。目前,KYV-101正在多种由B细胞介导的自身免疫性疾病中进行评估,重点关注SPS、重症肌无力和狼疮性肾炎。
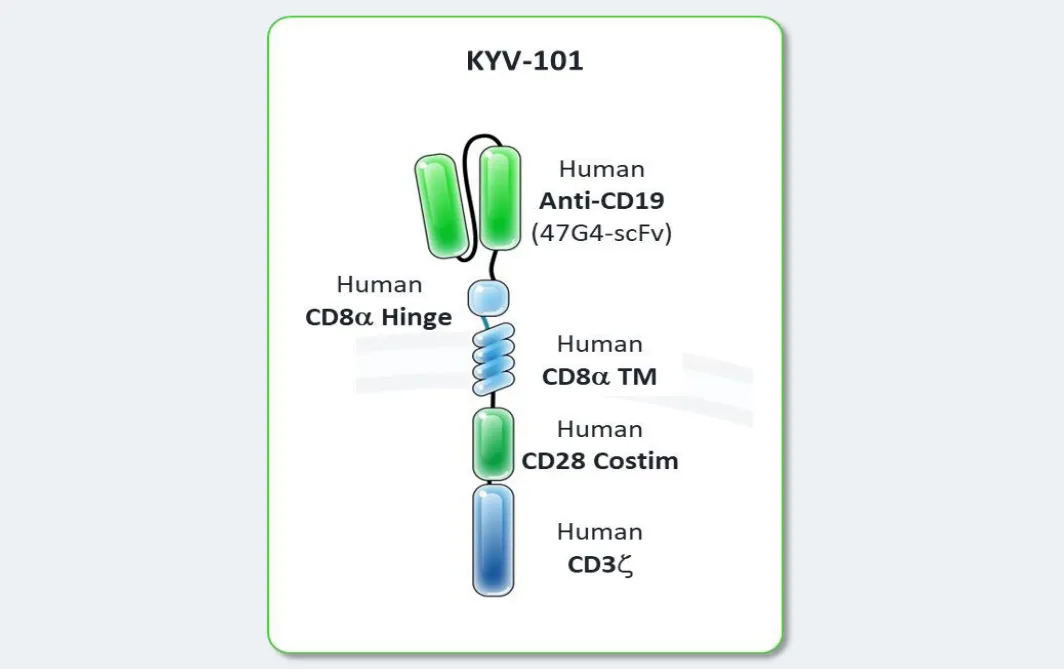
KYV-101的CAR构建体
miv-cel本次提交BLA的适应症是SPS,Kyverna已经和FDA达成一致,II期试验KYSA-8将作为KYV-101针对SPS的注册研究,包括25名患者的试验规模,其主要终点为25英尺步行(T25FW)测试。
Kyverna在2026年AAN年会上以口头报告的晚期口头报告,展示了关键KYSA-8试验的初步分析结果。报告显示:16周时所有主要和次要终点均具有统计学显著且持久的临床益处,miv-cel单次剂量后患者的残疾评分得以逆转。此外,截至第16周及最后随访,100%的患者均未接受SPS免疫治疗。
此外,在德国通过IH途径接受miv-cel单剂治疗的首批患者中,有两位分别取得了超过15个月和26个月的持久疗效,且无需长期接受免疫治疗。
Kyverna预计将于2026年下半年分享KYSA-8试验的一年随访数据。
FDA态度颇为积极
根据Kyverna公司披露,Kyverna与FDA的合作非常积极,而且在SPS上的观点是相互一致的,因为SPS目前尚无获批的药物,迫切需要尽快将新疗法带给患者。
Kyverna与FDA进行的pre-BLA会议进展积极,就miv-cel用于SPS的监管路径达成了一致,包括滚动提交BLA的材料以及BLA方案中的所有核心组成部分:注册性II期单臂试验KYSA-8的小样本数据足以支持miv-cel的SPS BLA申请,主要终点为16周的25英尺步行(T25FW)测试,以及临床安全方案、临床前资料包以及CMC包。
同时,Kyverna正在寻求miv-cel在再生医学先进疗法(RMAT)认证下的优先审查,预计将于2026年第四季度完成提交。
不过,目前Kyverna尚未获得完整方案,因为FDA要求提供更多信息。双方正在积极合作以确定最终所需的具体评估。应FDA要求,Kyverna将对自然历史研究进行额外的分析。
Kyverna的首席执行官Warner Biddle表示,这无需生成新的数据,只需利用现有数据进行额外分析。FDA并未对自然历史研究使用的方法提出任何质疑。Kyverna将在2026年美国神经学会年会上发表自研历史研究数据,以及KYSA-8的一年随访数据。
另外,在miv-cel提交上市申请的期间,FDA正在面临生物制品评估与研究中心(CBER)主任交接,Vinay Prasad离任,Katherine Szarama接任代理职务。但FDA CBER主任的交接,并未影响miv-cel的BLA提交。Kyverna表示,审查团队的一致性很高,预计领导人的变化不会改变原本的时间表。
小结
此外,基于FDA的积极态度以及可视的前景,Kyverna已经启动了miv-cel的商业化准备工作,包括商业站点激活、付款方参与及医疗专业人员(HCP)教育等。以及任命具有资深生物制药行业商业领导经验的Nadia Dac为首席商务官,以全力推动miv-cel未来的商业化布局。
如果miv-cel在未来顺利获得监管批准,将为CAR-T细胞治疗领域开辟一个新的商业化应用领域。当下,CAR-T细胞所获批的适应症都为肿瘤,自免领域的扩大将是CAR-T治疗的里程碑事件!

 产业资讯
产业资讯
 佰傲谷BioValley
佰傲谷BioValley  2026-05-14
2026-05-14
 442
442

 产业资讯
产业资讯
 丁香园Insight数据库
丁香园Insight数据库  2026-05-14
2026-05-14
 593
593

 产业资讯
产业资讯
 药智网
药智网  2026-05-14
2026-05-14
 487
487
 热门资讯
热门资讯